2025年4月11日,药品监管体系迎来重大变革,美国食品和药物管理局(FDA)发布历史性声明,计划逐步淘汰传统动物实验,转而采用实验室培养的类器官(organoids)和器官芯片(organ-on-a-chip)系统测试药物安全性,允许药企提交基于类器官和器官芯片的非动物实验数据作为审批依据,优先批准采用创新测试策略的企业。

FDA重磅:逐步取消动物实验
近10年类器官论文数量激增,但仅3%整合了蛋白质组学——你的课题是否还在“单组学裸奔”?

核心痛点:动物模型不靠谱?周期长?临床样本不够用?类器官+蛋白质组学,一键解决“无米之炊”+“机制脱节”两大难题!
类器官因其高度模拟真实器官结构与功能,正成为疾病建模与药物研发的新宠。然而,仅靠常规表征(如形态学观察或简单功能检测)难以全面评估类器官与真实体内环境的相似性。此时,蛋白质组学的引入成为关键——它从分子层面揭示类器官模型的真实性和可靠性,为研究提供更真实的数据支撑!
类器官是由干细胞或祖细胞在特定三维培养条件下自组织形成的、在结构和功能上部分模仿真实器官的微型结构。它们不仅能够模拟器官的发育过程,还能展现一定程度的生理功能。

类器官
更真实:3D结构+细胞异质性,秒杀传统二维细胞模型;
更精准:患者来源类器官(PDO)=“迷你替身”,推动精准医学;
更高效:在药物筛选与毒理学测试中,类器官提供了更可靠的预测能力。
类器官已逐渐成为连接基础研究与临床应用之间的重要桥梁。但如何验证其与真实体内情况的相似性?蛋白质组学是答案!
虽然类器官技术已广泛应用于多个领域,但将其与蛋白质组学技术结合的研究仍处于起步阶段。
数量较少,竞争不激烈:目前已发表的类器官+蛋白质组学的研究相对稀缺,尚未形成“卷”的态势;
文章质量高,易于冲击高分:已有的相关研究如发表于Nature, Cell, Science Translational Medicine等期刊的文章,表明这一方向具备发表重磅论文的潜力;

类器官&蛋白质组学文章期刊统计
技术挑战可控,方法体系逐渐成熟:随着微量样本蛋白质组学(如单细胞蛋白质组学和空间蛋白质组学)的发展,类器官样本的蛋白组研究已不再“难以下口”。
当前正是切入类器官+蛋白质组学研究的黄金窗口期!!!
常规表征(如形态学或功能检测)只能提供表面信息,而蛋白质组学能从分子层面全面评估类器官与原组织的相似性。例如:
通过差异蛋白分析,验证类器官是否保留了原组织的关键信号通路和功能蛋白;
通过修饰蛋白质组学(如磷酸化、糖基化),揭示类器官的细胞状态是否与体内一致。
2025年2月,挪威科技大学Chun-Mei Zhao教授团队在期刊Scientific Data(IF=5.8)在线发表题为:Proteomics profiling of research models for studying pancreatic ductal adenocarcinoma的高水平研究论文。本研究通过蛋白质组学分析比较了类器官与原始样本(包括小鼠和人类的胰腺癌(PDAC)细胞、球体、类器官和组织)之间的相似性和差异性。结果显示,类器官在蛋白质表达谱、形态学和功能特性上与原始肿瘤组织表现出较高的相似性,能够模拟肿瘤的化疗药物耐药性、高增殖活性和低凋亡活性等关键特征。然而,类器官在某些蛋白质的表达上与原始肿瘤组织存在差异,这可能与类器官的培养环境和缺乏完整的肿瘤微环境有关。尽管如此,类器官仍可作为研究PDAC的重要模型,但使用时需注意这些差异,并通过优化培养条件和结合多种模型进行综合分析,以提高其研究价值[1]。
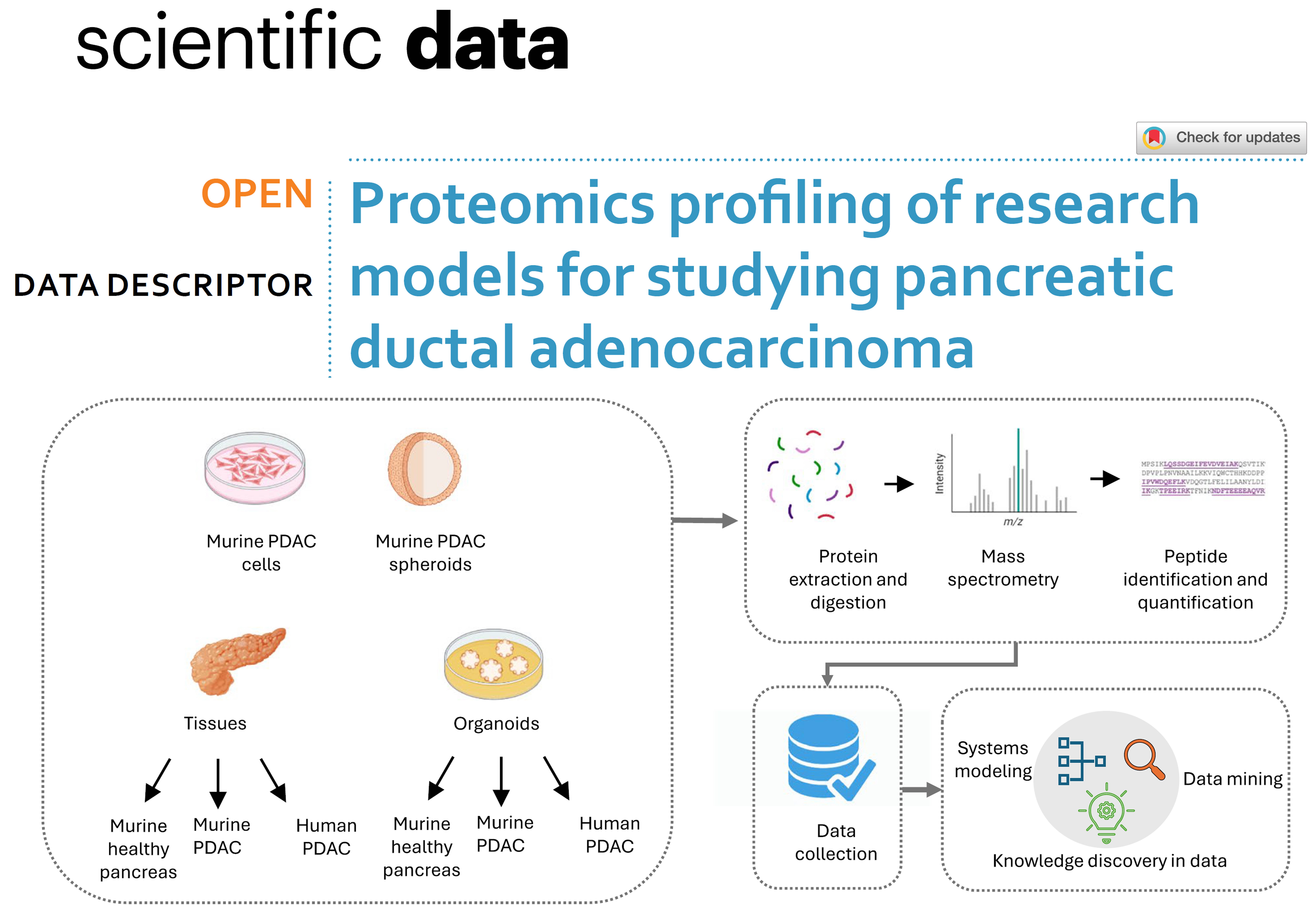
疾病建模革命:疾病类器官模型的蛋白质组学描绘与一致性评价
你的机会:肿瘤/神经/肠道类器官+蛋白组=下一个“疾病标志物”的诞生地!
类器官作为“微型患者模型”,在药物干预实验中展现出更高的预测性。在对类器官进行药物处理或基因干预后,蛋白质组学能系统捕捉分子层面的动态变化,从而:
揭示药物靶点、耐药机制或毒性反应的关键蛋白;
构建动态蛋白网络,发现隐藏的调控枢纽。
2025年3月,中国医学科学院北京协和医院冷泠团队在Nature子刊Nature Communications(IF=14.7)上发表了题为:A skin organoid-based infection platform identifies an inhibitor specific for HFMD的研究论文。该研究开发了一种基于人类诱导多能干细胞来源的皮肤类器官(hiPSC-SO)感染平台,锁定自噬/Hippo-YAP通路为抗病毒靶点,成功鉴定出了手足口病(HFMD)的特异性抑制剂[2]。
在这项最新研究中,研究团队以人类诱导多能干细胞来源的皮肤类器官(hiPSC-SO)作为EV-A71 感染的模型,首次构建了EV-A71感染皮肤类器官的单细胞RNA测序(scRNA-seq)和蛋白质组学分析,以研究EV-A71感染的毒力、分子特征和发病机制,发现了皮肤类器官内的多种细胞类型,包括表皮细胞、毛囊细胞、成纤维细胞和神经细胞,均表达EV-A71受体,并且易受EV-A71感染,并进一步揭示了其中成纤维细胞和表皮细胞是EV-A71的主要靶细胞,EV-A71感染可降解细胞外胶原蛋白,从而可能加速皮肤衰老。
该研究还发现,EV-A71可通过细胞自噬以及整合素/Hippo-YAP/TAZ信号通路介导表皮细胞损伤,从而促进祖细胞的过度增殖,可能促进肿瘤发生。
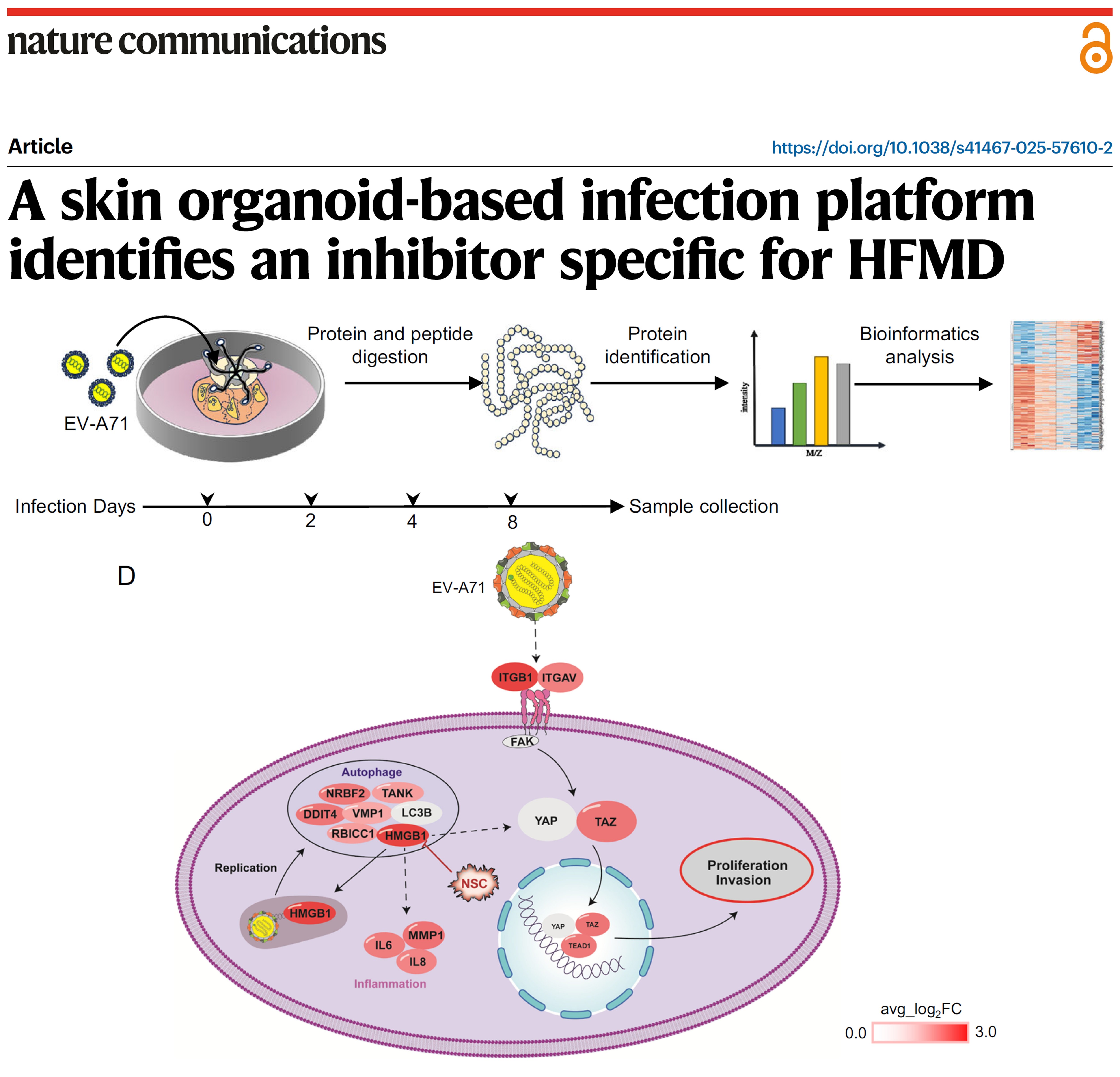
药物研发开挂:药物作用机制与耐药机制解析
你的机会:耐药性解析、老药新用,高分文章“流水线”已就绪!
方向1:类器官vs原组织的蛋白表达一致性评估(参考2025 Scientific Data胰腺癌研究)
方向2:药物扰动下的动态蛋白网络(如化疗耐药性时空图谱)
定量蛋白质组学+修饰蛋白质组学+单细胞测序=多维数据炸裂输出!
药物靶点研究(热蛋白质组学TPP/限制性酶解-质谱分析LiP-MS)+湿实验验证=闭环研究逻辑,审稿人无法拒绝!
类器官培养易翻车?一站提供类器官培养+蛋白质组学检测服务!
类器官与蛋白质组学的融合不仅是技术上的“强强联合”,更是通向精准医学与机制研究深水区的有力武器。分子层面的表征让模型更真实,干预后的蛋白动态让数据更真实。
无论你是基础研究者,还是临床科研人员,类器官+蛋白组学或许正是你冲击高水平成果的下一个机会窗口。如果你想要进一步探索如何设计类器官+蛋白质组学实验,或者如何结合多组学进行整合分析,欢迎留言交流~
[1] <202502-Sci Data-Proteomics profiling of research models for studying pancreatic ductal adenocarcinoma.pdf> [J].
[2] LI J, MA J, CAO R, et al. A skin organoid-based infection platform identifies an inhibitor specific for HFMD [J]. Nature Communications, 2025, 16(1).