T细胞耗竭是肿瘤免疫治疗(如CAR-T、免疫检查点抑制剂)面临的主要障碍之一。耗竭T细胞(TTEX)表现为效应功能丧失、抑制性受体(如PD-1、TIM3)高表达、干细胞样特性丧失。耗竭 T 细胞会累积去极化线粒体,且线粒体自噬受损;去极化线粒体可调控基因转录、促进 T 细胞终末分化,但具体分子机制完全未知。
2026 年3月18日,中国医学科学院血液病医院王建祥教授及徐颖茜副研究员,瑞士洛桑大学何秉智教授团队合作在顶刊《Nature》(IF:48.5)发表文章“ Proteasome-guided haem signalling axis contributes to T cell exhaustion”。该研究首次揭示线粒体去极化→CBLB 介导泛素化→蛋白酶体选择性降解→血红素释放→BACH2 降解→T 细胞终末耗竭的完整机制,首次将泛素 - 蛋白酶体系统置于 T 细胞耗竭调控的核心位置,完成从基础机制到 CAR-T 临床转化的全链条验证,并基于该机制提出蛋白酶体抑制剂优化 CAR-T 的临床转化策略。
北京青莲百奥生物科技有限公司提供了泛素化蛋白组学检测服务。 研究亮点速递
研究亮点速递
1.全新机制发现:首次建立线粒体 - 泛素化-蛋白酶体 - 血红素 - BACH2的 T 细胞耗竭调控轴,填补线粒体功能异常驱动 T 细胞耗竭的分子机制空白。
2.关键靶点鉴定:明确CBLB(E3 泛素连接酶)、PGRMC2(血红素核转运蛋白)、BACH2是调控该轴的核心分子。
3.多组学验证:结合泛素化蛋白组、转录组、单细胞多组学、ATAC-seq 等技术,在小鼠、人 T 细胞、临床样本中完成全方位验证。
4.临床转化突破:证实FDA 获批的蛋白酶体抑制剂硼替佐米(阻断泛素化引发的蛋白降解)可在 CAR-T 制备阶段抑制耗竭、提升抗肿瘤疗效;CAR-T 细胞的蛋白酶体特征可作为疗效预测标志物。
研究结果
1、泛素化组学揭示:终末耗竭T细胞选择性降解线粒体蛋白
该研究分析黑色素瘤、头颈鳞癌、肺癌患者肿瘤浸润 T 细胞(TIL)的单细胞数据,发现终末耗竭 T 细胞(TTEX)的蛋白酶体通路显著富集,体外分化人 CD8+ T 细胞亚群也证实TTEX 细胞蛋白酶体活性远高于 祖细胞耗竭T细胞(TPEX)、记忆 T 细胞。
因此检测泛素化蛋白质组发现:与效应T细胞相比,终末耗竭T细胞中泛素化修饰显著富集于线粒体蛋白;而记忆T细胞则优先泛素化胞质蛋白。这一差异揭示了终末耗竭T细胞线粒体特异性泛素化降解机制。随后分选出去极化线粒体 T 细胞(MDR/MGlow),其蛋白酶体相关蛋白表达显著升高,且优先降解线粒体蛋白。并进一步验证到去极化线粒体通过上调E3 泛素连接酶 CBLB,触发蛋白酶体对线粒体蛋白的选择性降解。
结论:去极化线粒体累积→CBLB 激活泛素化→蛋白酶体选择性降解线粒体蛋白,是耗竭 T 细胞的代偿性稳态机制,但会引发后续耗竭级联反应。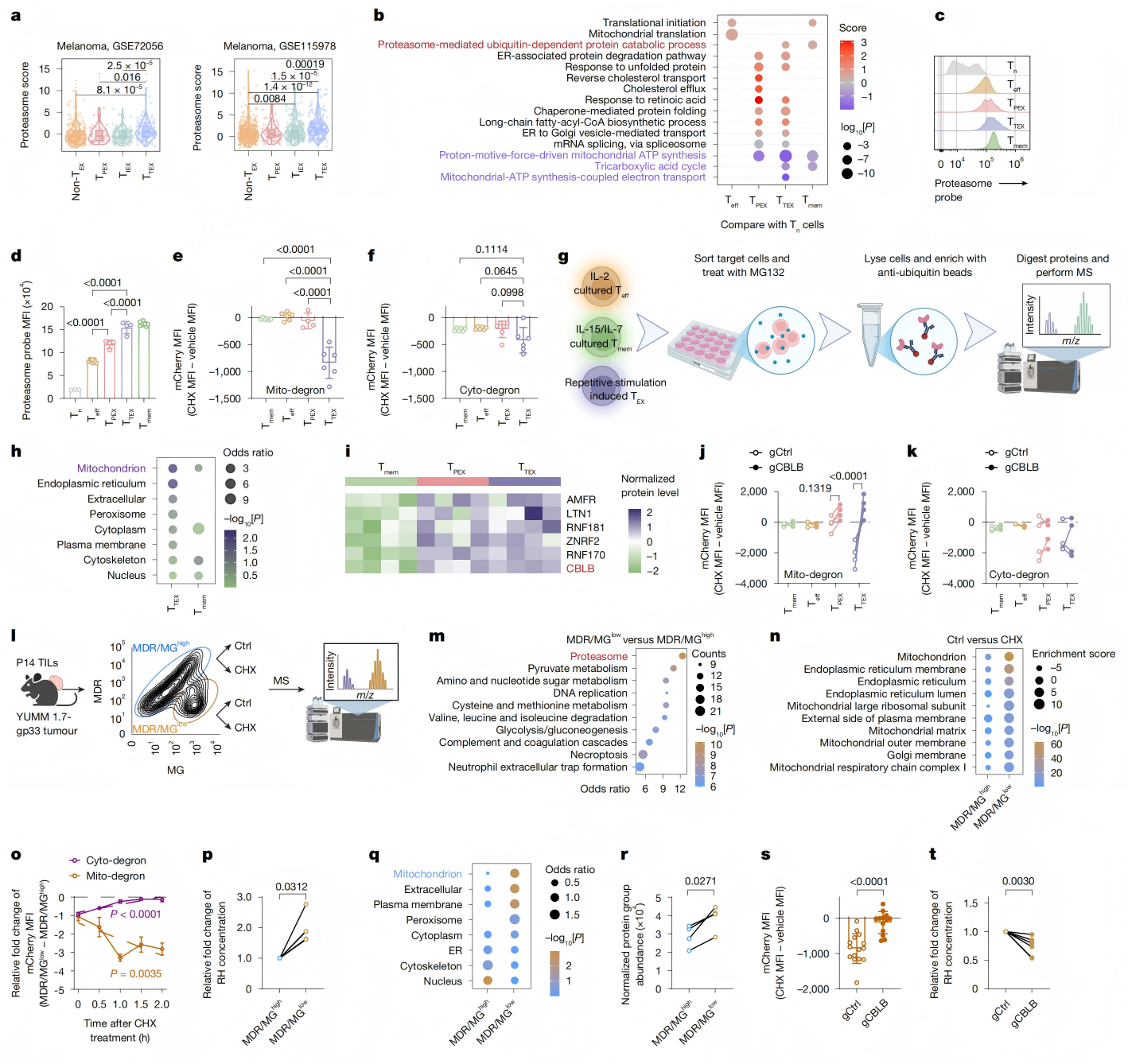 2、泛素化降解介导大量血红素(RH)释放,直接诱导 T 细胞终末耗竭
2、泛素化降解介导大量血红素(RH)释放,直接诱导 T 细胞终末耗竭
线粒体蛋白中大量为血红素结合蛋白,其降解会释放 RH。检测发现去极化线粒体 T 细胞、TTEX 细胞的 RH 水平显著升高,蛋白酶体抑制剂可降低 RH。此外,肿瘤间质液的 RH 水平高于血清,提示肿瘤微环境(TME)加剧 RH 累积。
随后,用血红素类似物氯高铁血红素(haemin)处理 T 细胞,发现其抑制增殖、降低 IFN-γ/TNF 分泌、上调 PD-1/TIM3、下调 TCF-1/CD62L,完全模拟终末耗竭表型。
结论:泛素 - 蛋白酶体介导的线粒体血红素蛋白降解→RH 异常累积,是驱动 CD8+ T 细胞终末耗竭、丧失干性的直接诱因。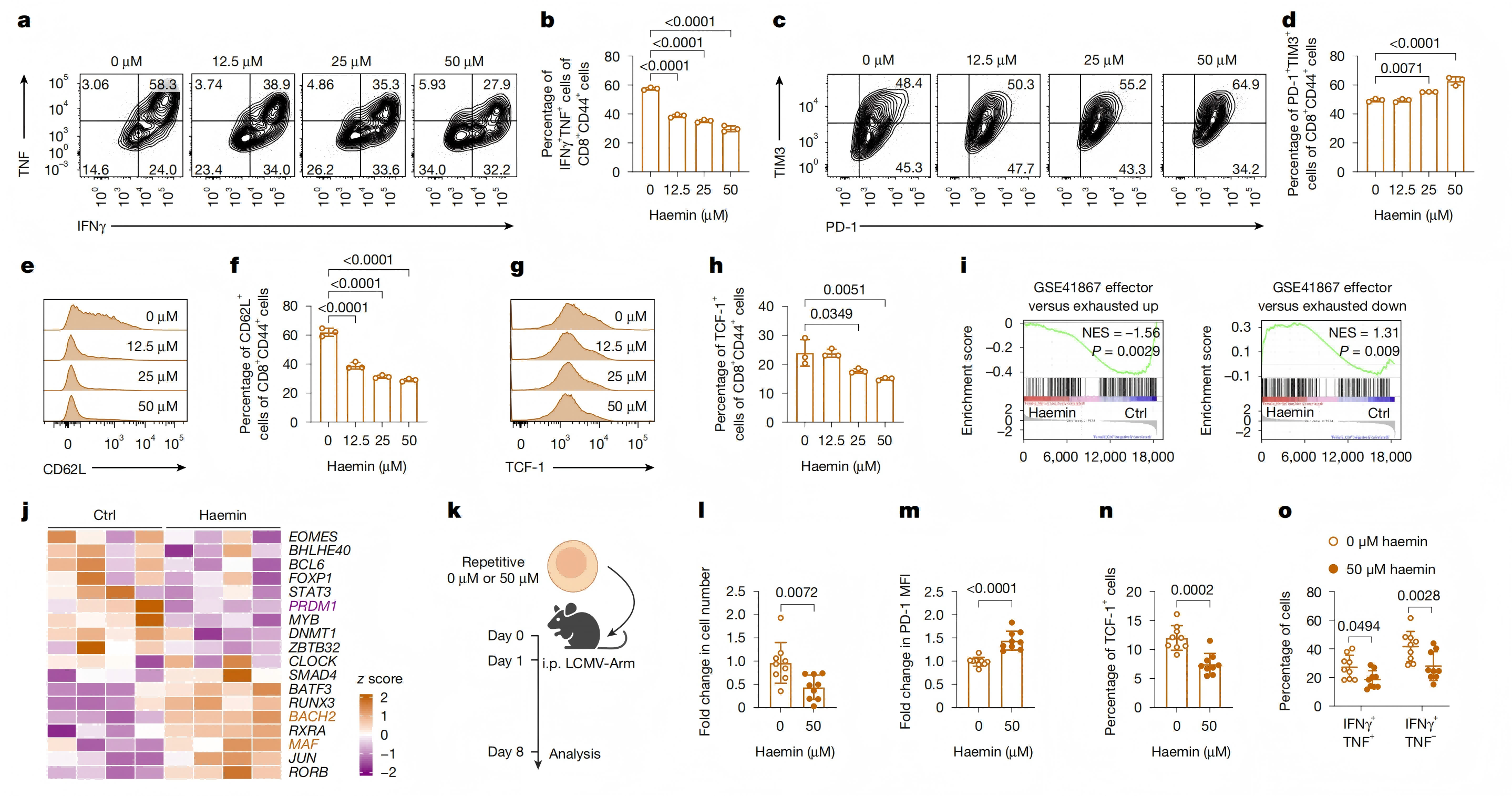 3、血红素通过 BACH2-BLIMP1 轴调控 T 细胞命运
3、血红素通过 BACH2-BLIMP1 轴调控 T 细胞命运
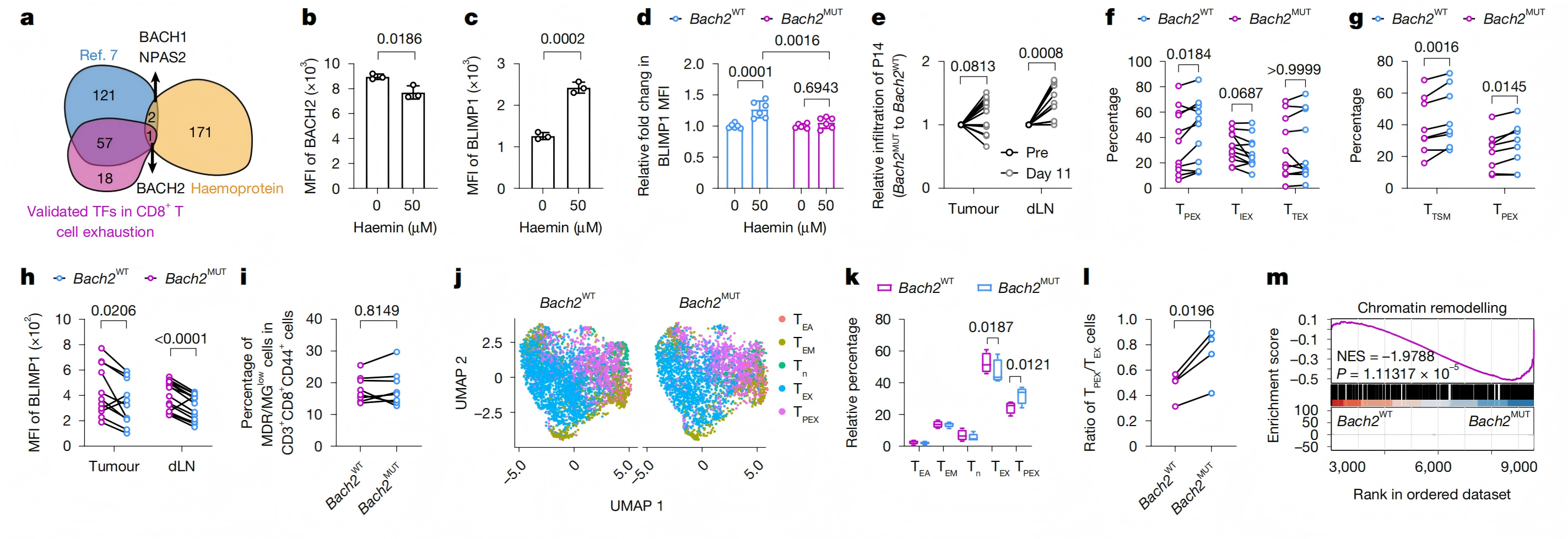
为了锚定关键转录因子,该研究交叉分析血红素结合蛋白、T 细胞耗竭转录因子、CRISPR 筛选耗竭调控因子,唯一交集为BACH2(维持 TPEX 干性的核心转录因子)。构建血红素结合位点突变的 BACH2(BACH2MUT),其可抵抗血红素介导的降解,持续抑制 BLIMP1。回输 BACH2MUT T 细胞至荷瘤小鼠做体内干性维持验证,结果表明TPEX 比例显著升高、TTEX 减少,干性相关基因高表达,且不依赖线粒体功能修复。
结论:RH 结合并降解 BACH2→BLIMP1 上调,是血红素驱动 T 细胞从 TPEX 向 TTEX 转换的核心分子通路。
4、阻断血红素核转运,恢复 T 细胞抗肿瘤功能
PGRMC2 是血红素核转运分子伴侣,敲除 PGRMC2 可阻止 RH 进入细胞核,不改变细胞总血红素水平。此外,PGRMC2 敲除的 T 细胞:BACH2 稳定、BLIMP1 下调、细胞因子分泌增强、线粒体功能改善。荷瘤小鼠回输 PGRMC2 敲除的 T 细胞 / HER2 CAR-T,肿瘤生长显著延缓、小鼠生存期延长。
结论:靶向 PGRMC2 阻断血红素核转运,可恢复 BACH2-BLIMP1 平衡、提升线粒体健康、增强 T 细胞抗肿瘤效应,是全新的免疫治疗靶点。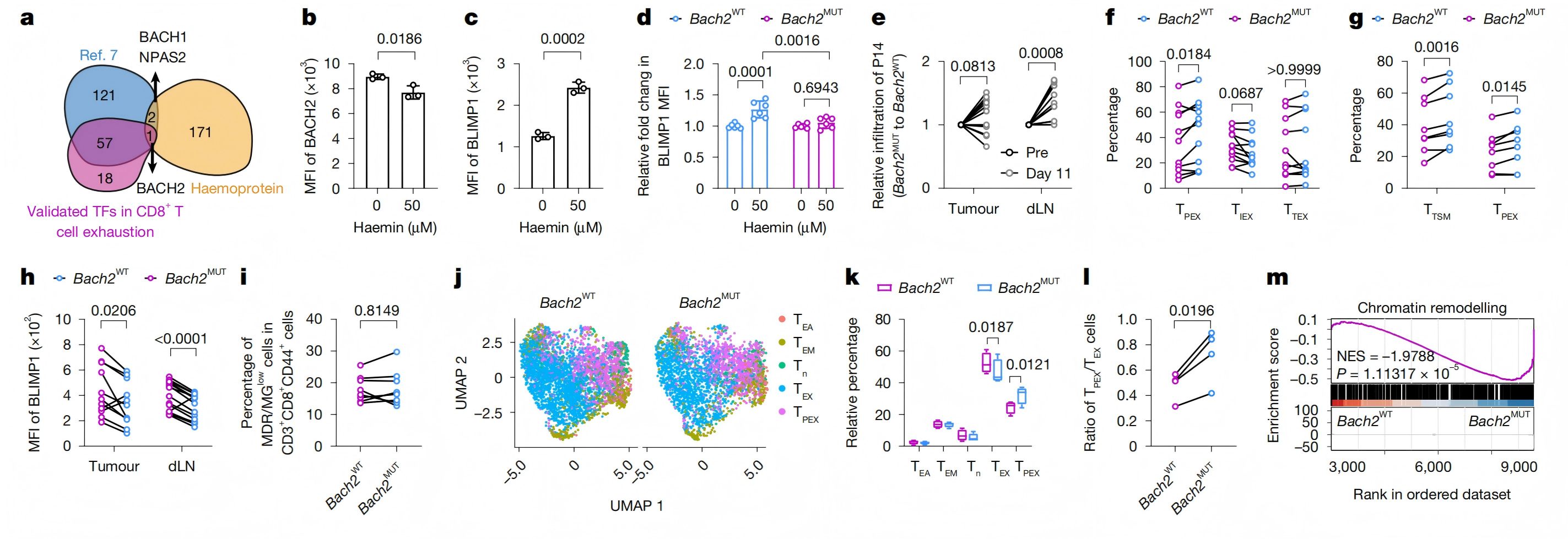 5、泛素-蛋白酶体调控优化 CAR-T 细胞,临床转化验证
5、泛素-蛋白酶体调控优化 CAR-T 细胞,临床转化验证
随后该研究使用临床样本关联分析,分析 6 例 B-ALL 患者 CD19 CAR-T 细胞,完全缓解患者的 CAR-T 以记忆样亚群为主,复发患者以耗竭亚群(Cytot-GZMB)为主。用低剂量硼替佐米(FDA 获批蛋白酶体抑制剂)预处理 CAR-T 细胞,可降低 PD-1+TIM3+CD39 + 耗竭亚群比例。回输至白血病小鼠,体重稳定、生存期显著延长。
多组学分析结果表明,硼替佐米预处理诱导持久表观遗传重编程:上调记忆 / 干性相关转录因子(KLF2、FOXO1),下调耗竭相关因子(BLIMP1、ETS1)。促进氨基酸摄入、IL-4 信号通路,增强 CAR-T 记忆与效应功能。
结论:CAR-T 制备阶段用低剂量硼替佐米抑制蛋白酶体系统,可阻断耗竭、提升临床疗效,具备快速临床转化价值。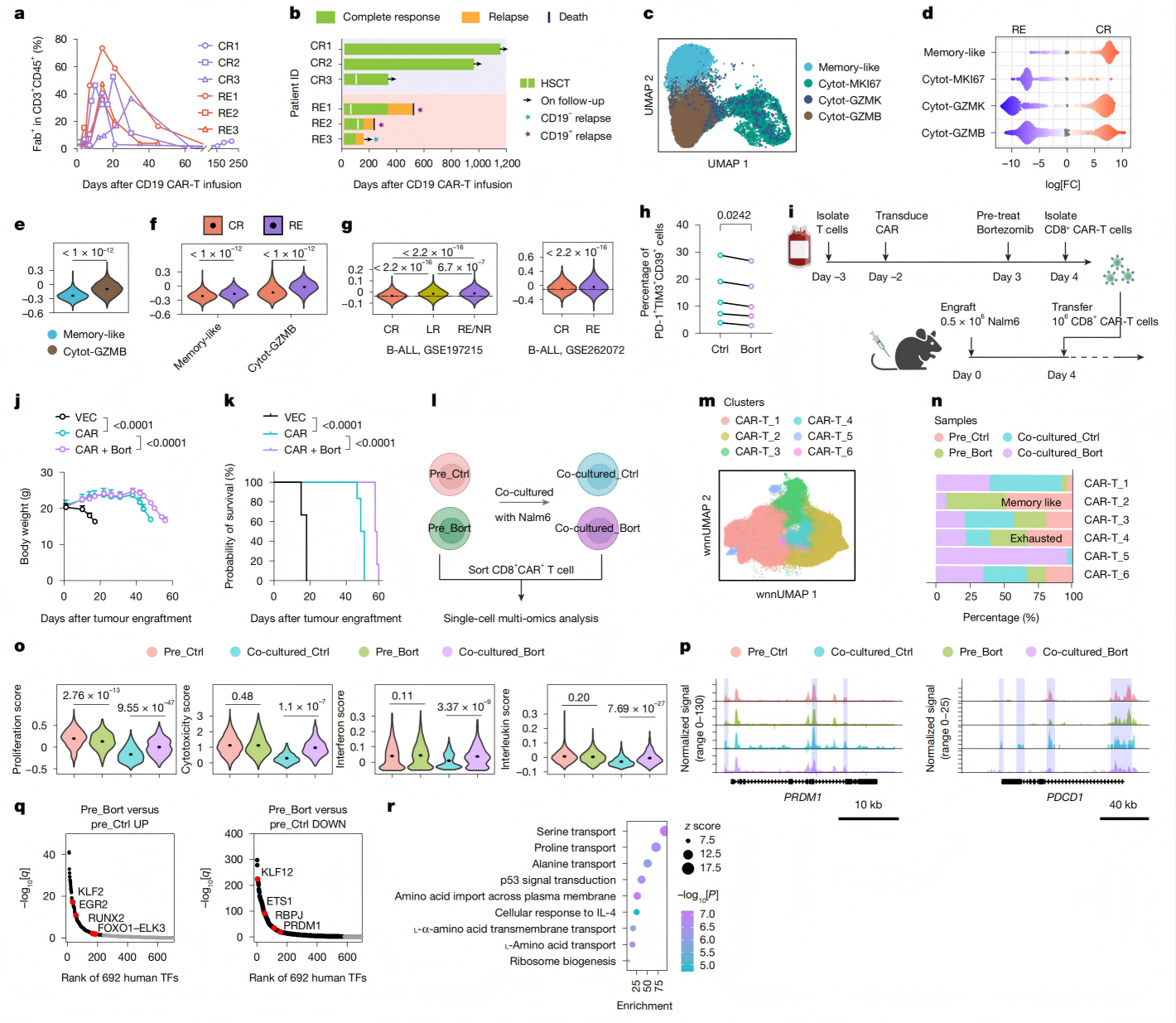 研究结论与意义
研究结论与意义
该研究首次强调了泛素化修饰是T细胞衰竭的关键起点之一,阐明线粒体去极化通过 CBLB 介导的泛素化修饰,激活蛋白酶体对线粒体血红素蛋白的选择性降解,释放的调节性血红素经 PGRMC2 转运入核,结合并降解干性转录因子 BACH2、上调 BLIMP1,最终驱动 CD8⁺ T 细胞走向终末耗竭。而在 CAR-T 制备阶段使用低剂量硼替佐米抑制蛋白酶体,可显著减少细胞耗竭、增强记忆干性并提升抗肿瘤效果。
这项工作填补了线粒体功能异常驱动 T 细胞耗竭的分子机制空白,首次将泛素 - 蛋白酶体系统、血红素代谢与转录调控耦联,为 T 细胞免疫代谢提供全新理论框架。更重要的是提出可快速转化的 CAR‑T 优化策略,将蛋白酶体评分作为疗效标志物、用已上市药物改善 CAR‑T 持久性,为实体瘤免疫治疗带来全新方向。
青莲百奥修饰组学解决方案
青莲百奥修饰蛋白组学产品线升级,不仅精心打磨了经典修饰产品线(如磷酸化、糖基化、泛素化等),同时开拓了一系列新型修饰产品线(如乳酸化、棕榈酰化、琥珀酰化、氧化还原等)。现凭借先进的高分辨率、高灵敏度质谱技术,积累了丰富的修饰组学研究经验,提供深入的生物信息学分析报告,为科研工作的深入探索和成果的有效转化提供强有力的支持。
