EV-A71:隐藏在皮肤接触背后的“杀手”
作为手足口病(HFMD)的主要致病病毒,EV-A71可通过直接或间接的皮肤接触迅速传播,严重威胁儿童的健康甚至生命安全。然而,目前对其在皮肤层面的传播机制与致病过程仍知之甚少。如何在“第一道防线”上揭示病毒的真实面目?基于人源细胞构建全新皮肤模型,正成为破解病毒奥秘、推动抗病毒药物筛选与开发的关键突破口。

2025年3月13日中国医学科学院北京协和医院冷泠研究员团队在Nat Commun(IF=14.7)杂志上发表了题为“A skin organoid-based infection platform identifies an inhibitor specific for HFMD”的论文。该研究创建了人诱导多能干细胞来源的皮肤类器官(hiPSC-SOs)感染模型,利用单细胞转录组测序和蛋白质组学技术,结果发现EV-A71可以通过自噬和Integrin/Hippo-YAP/TAZ信号通路介导表皮细胞损伤,从而促进祖细胞的过度增殖。基于该发现,确定了一种自噬相关蛋白作为EV-A71的药物靶标,并发现了一种EVA71复制抑制剂为手足口疾病的临床治疗提供了新的有益方向[1]。

蛋白质组学的关键作用
文章开展蛋白质组学分析,旨在系统解析EV-A71感染后hiPSC皮肤类器官中的分子机制和病理变化。
1. 通过不同时间点(2、4、8天)的动态分析,揭示病毒如何调控宿主的病毒复制、自噬、免疫应答、基质降解等关键生物过程。
2. 同时,蛋白质组数据与单细胞测序联合使用,帮助识别了HMGB1这一关键宿主因子,并验证其为潜在的抗病毒治疗靶点。该策略为深入理解病毒致病机制和靶向药物开发提供了有力支持。
关键结果
皮肤类器官模型成功建立
本研究通过优化hiPSC的逐步分化方案,成功构建了包含表皮细胞、毛囊细胞和神经细胞的皮肤类器官模型(hiPSC-SOs)。免疫荧光检测证实,这些细胞均表达EV-A71的关键受体(SCARB2、ANXA2等)。通过时间梯度感染实验(2、4、8天)发现,病毒载量随感染时间呈显著上升趋势(p<0.05),证实hiPSC-SOs对EV-A71具有高度易感性,为后续机制研究提供了可靠平台。
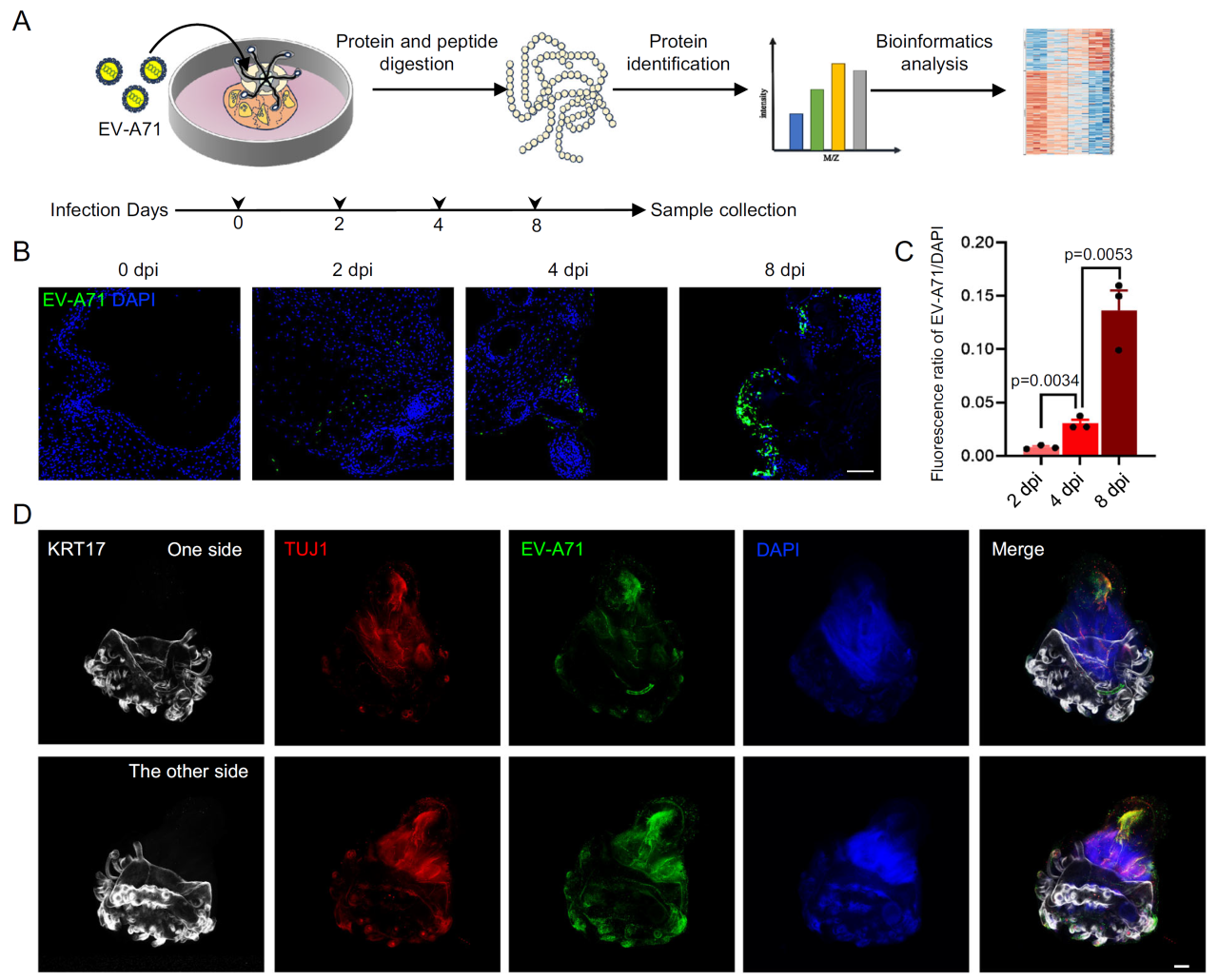
hiPSC-SO易受EV-A71感染
EV-A71感染hiPSC-SO的蛋白质组时态动态变化
研究通过对EV-A71感染后2天、4天和8天的hiPSC-SO进行蛋白质组学分析,揭示了病毒感染的阶段性特征:
早期(2天):病毒复制相关蛋白(如病毒基因组复制、DNA复制)上调,显示宿主细胞协助病毒增殖。
中期(4天):糖酵解和葡萄糖转运蛋白增加,表明细胞能量代谢增强以支持病毒复制。
晚期(8天):免疫反应、细胞因子响应及缺氧相关蛋白激活,反映炎症和组织损伤。
这些变化表明EV-A71感染逐步破坏皮肤正常功能,为靶向治疗提供了依据。
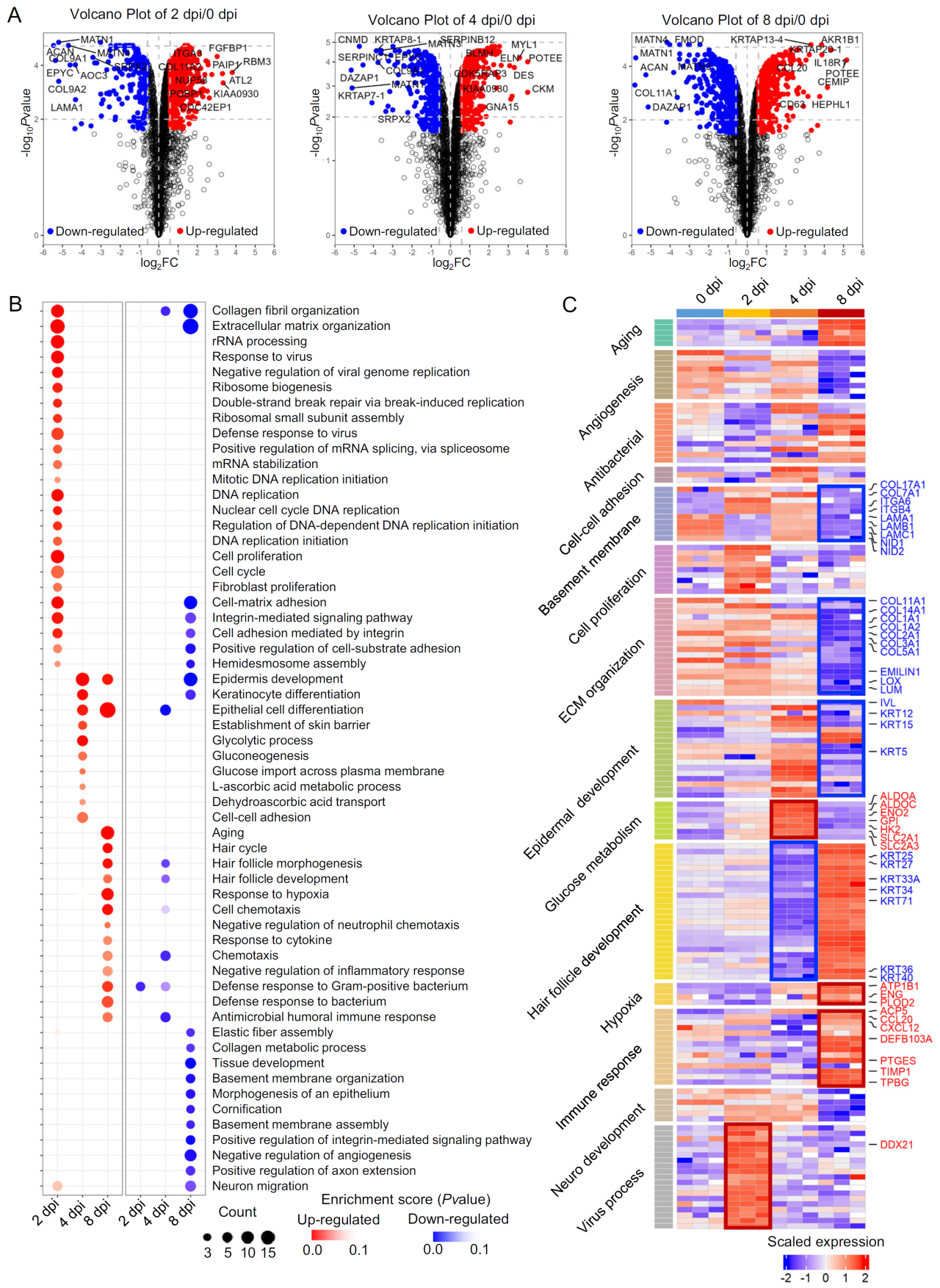
EV-A71通过hiPSC-SOs中的自噬途径介导表皮细胞功能障碍
EV-A71的感染hiPSC-Sos的作用机制
为系统研究EV-A71感染对hiPSC来源皮肤类器官(hiPSC-SOs)的生物学影响,研究团队综合应用单细胞RNA测序(scRNA-seq)与蛋白质组学技术,揭示了病毒感染在细胞类型特异性水平上的病理机制。分析结果显示,网状成纤维细胞在感染后显著减少,病毒通过激活TNF-α信号通路,诱导上调多种基质金属蛋白酶(MMP1、MMP3、MMP13),导致胶原蛋白降解和细胞外基质结构破坏,提示其可能加速皮肤老化过程。与此同时,表皮祖细胞(NNMT⁺ SFRP1⁺ PCs)在病毒感染后发生异常增殖,研究发现该过程与整合素介导的Hippo-YAP/TAZ信号通路持续激活密切相关,可能促进病毒诱导的肿瘤样转化。此外,病毒感染还引发HMGB1的持续上调,进而激活自噬通路(LC3B表达升高),为病毒自身的复制提供支持。整体来看,EV-A71通过多条关键通路协同扰乱皮肤组织稳态,诱发炎症、结构破坏与细胞功能紊乱,为其致病机制和抗病毒靶点提供了理论基础。
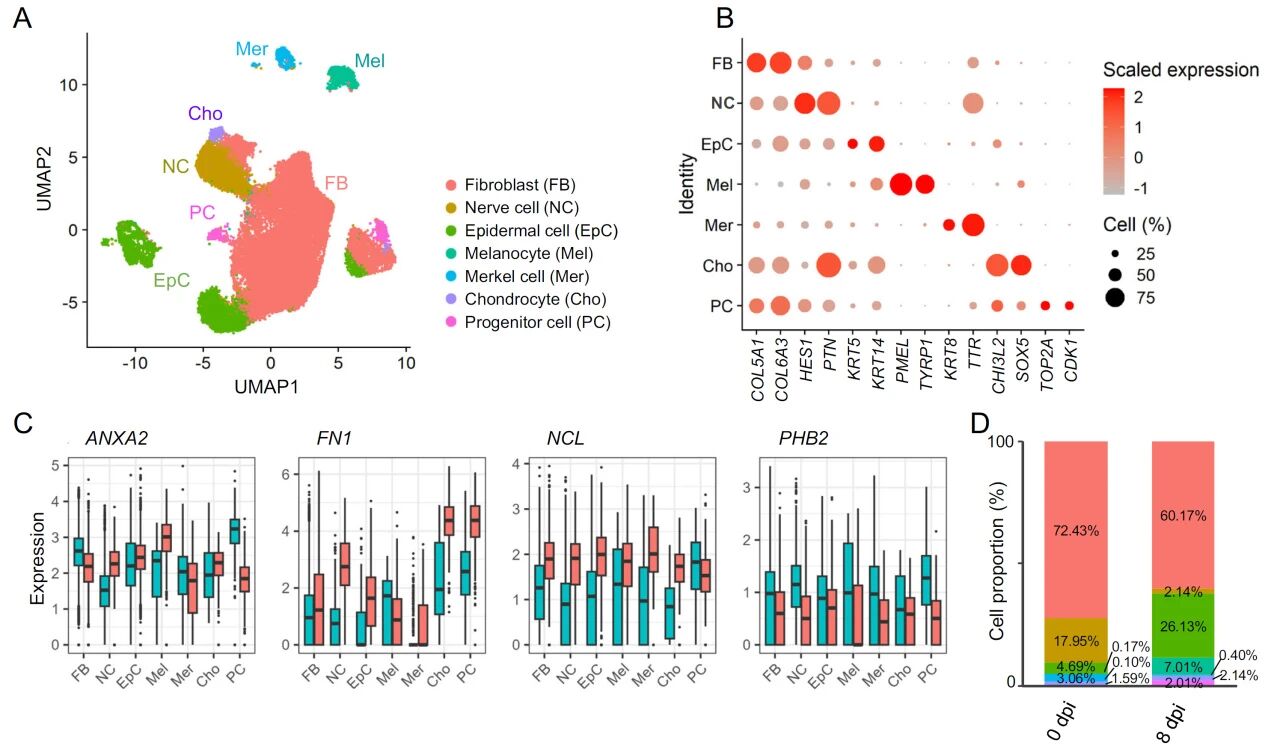
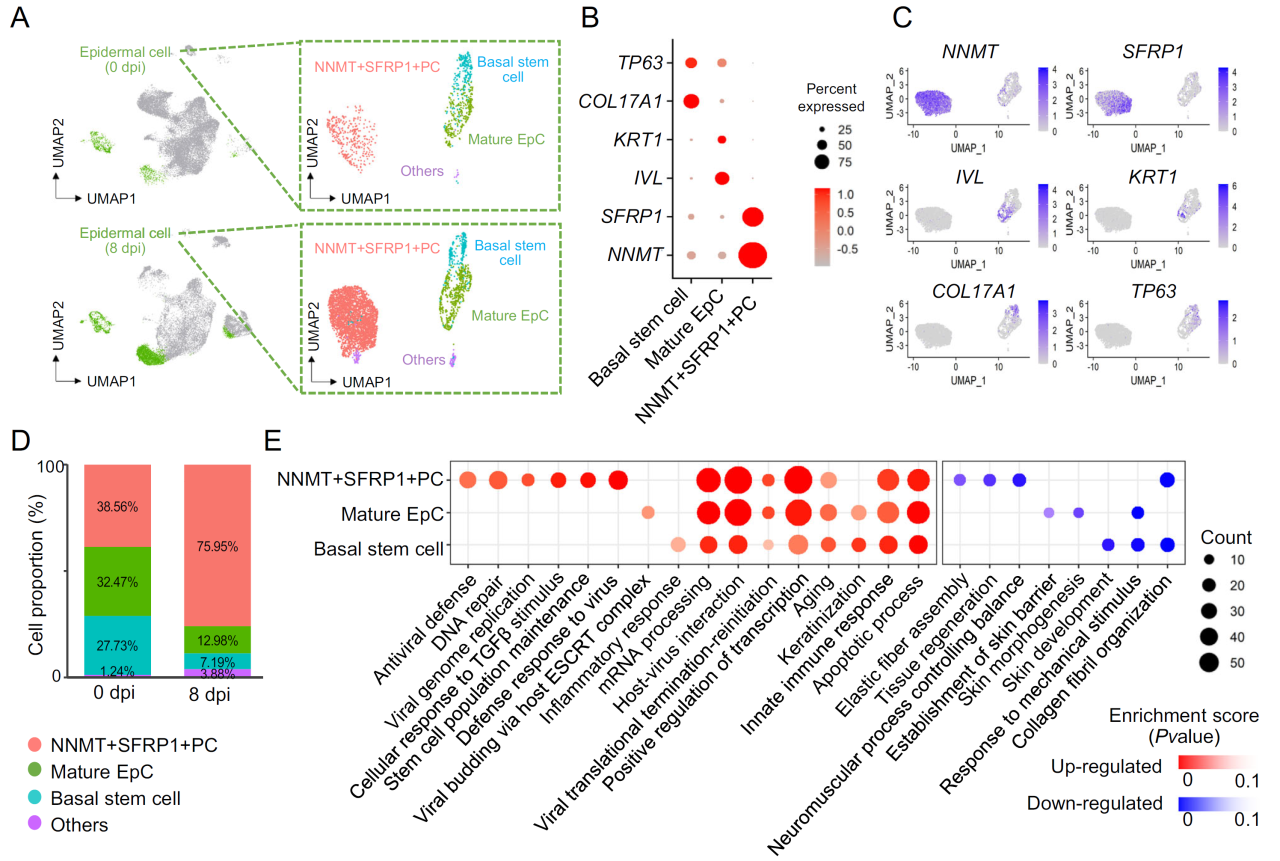
EV-A71病毒感染导致网状成纤维细胞耗竭,祖细胞增殖
药物筛选与验证
在本研究中,基于蛋白质组与单细胞转录组的联合分析,HMGB1被鉴定为EV-A71感染过程中的关键宿主因子,其在多种易感细胞类型中表达显著上调,并与病毒复制水平呈正相关。进一步的功能验证表明,针对HMGB1的FDA批准抑制剂NSC167409(甘草酸衍生物)在体外(Vero和RD细胞)和体内(人源化hiPSC-SO移植物小鼠模型)均表现出显著的抗病毒活性。药物处理不仅有效抑制病毒复制,同时还显著降低了病毒诱导的表皮祖细胞(NNMT⁺ SFRP1⁺ PCs)异常增殖和炎症因子表达,如IL-6与MMP家族。药效评估显示,NSC167409的IC₅₀为1.02μM,远低于其已知血浆峰值浓度(29.25μg/mL),提示该药物具有良好的药代动力学特性和临床应用潜力。
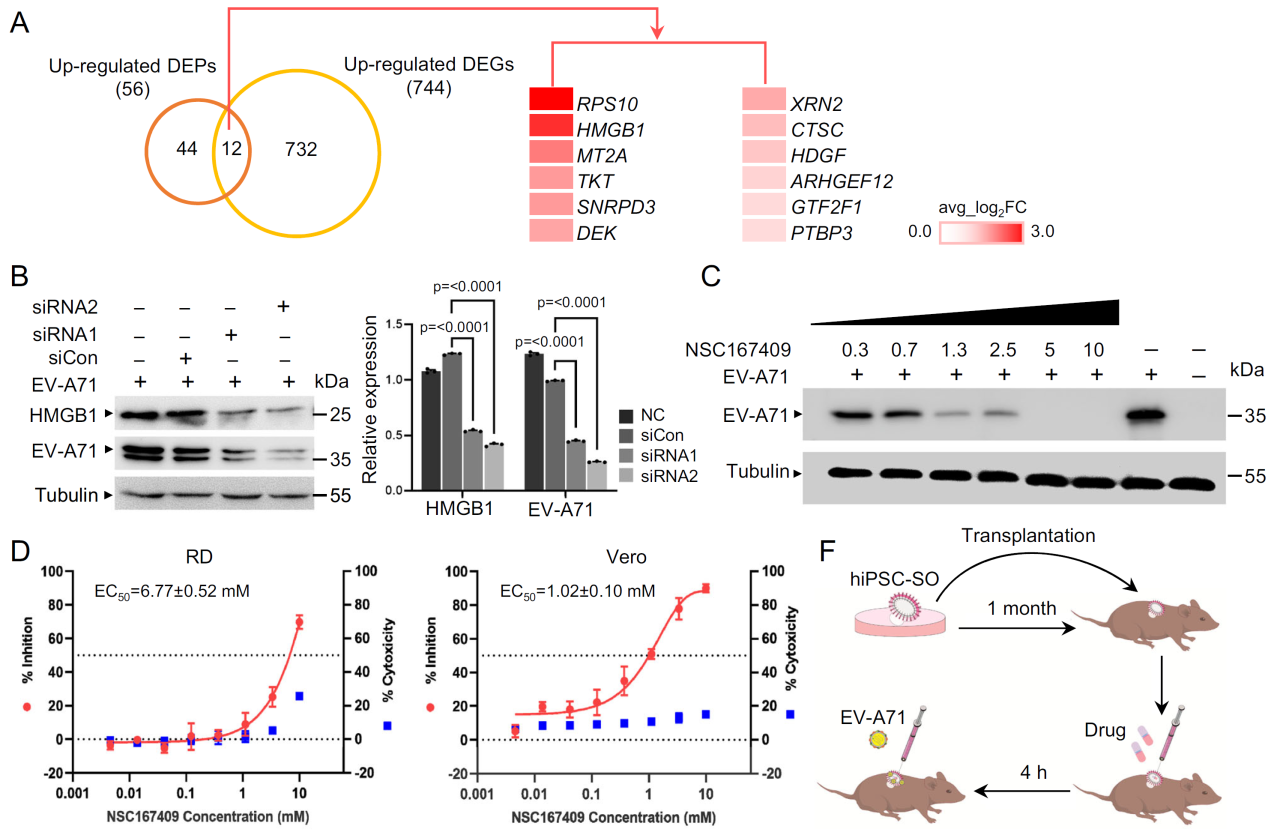
NSC167409在体内外均能阻断EV-A71复制
文章结论
本研究基于hiPSC皮肤类器官模型,通过蛋白质组学揭示EV-A71感染引发的时间依赖性分子变化。结果显示,病毒激活自噬、病毒复制等通路,同时抑制胶原合成和皮肤结构蛋白表达,破坏组织稳态。整合分析发现HMGB1为关键调控因子,其抑制剂NSC167409可有效阻断病毒复制并缓解炎症,体现了蛋白质组学在靶点发现与药物筛选中的重要价值。
研讨会直播预约ING
6月26日下午14:00,一场关于未来医学的头脑风暴即将开启!
由青莲百奥×丹望医疗联合主办的【类器官×蛋白质组学:精准医疗新引擎】线上直播重磅来袭!
高深度蛋白质组学分析
类器官模型在临床研究中的应用
最前沿技术与真实案例分享
精准医疗从不止步,科研探索永无止境。我们诚邀每一位关注前沿生物医学的您,共赴这场云端学术盛宴!
参考文献:
[1] LI J, MA J, CAO R, et al. A skin organoid-based infection platform identifies an inhibitor specific for HFMD [J]. Nature Communications, 2025, 16(1).