近年来,肿瘤代谢与免疫调控之间的关系成为研究热点。乳酸化修饰由肿瘤糖酵解代谢的关键产物乳酸所形成,但其与肿瘤免疫调控的关系仍不清楚。
2026年3月21日,浙江大学吴明团队在Cell Death & Disease(IF 9.6/Q1)上发表题为“Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth”的研究论文,系统解析了糖酵解驱动的乳酸化如何调控PD-L1稳定性,从而促进肿瘤免疫逃逸与生长,为提升免疫治疗疗效提供了全新的思路和靶点。
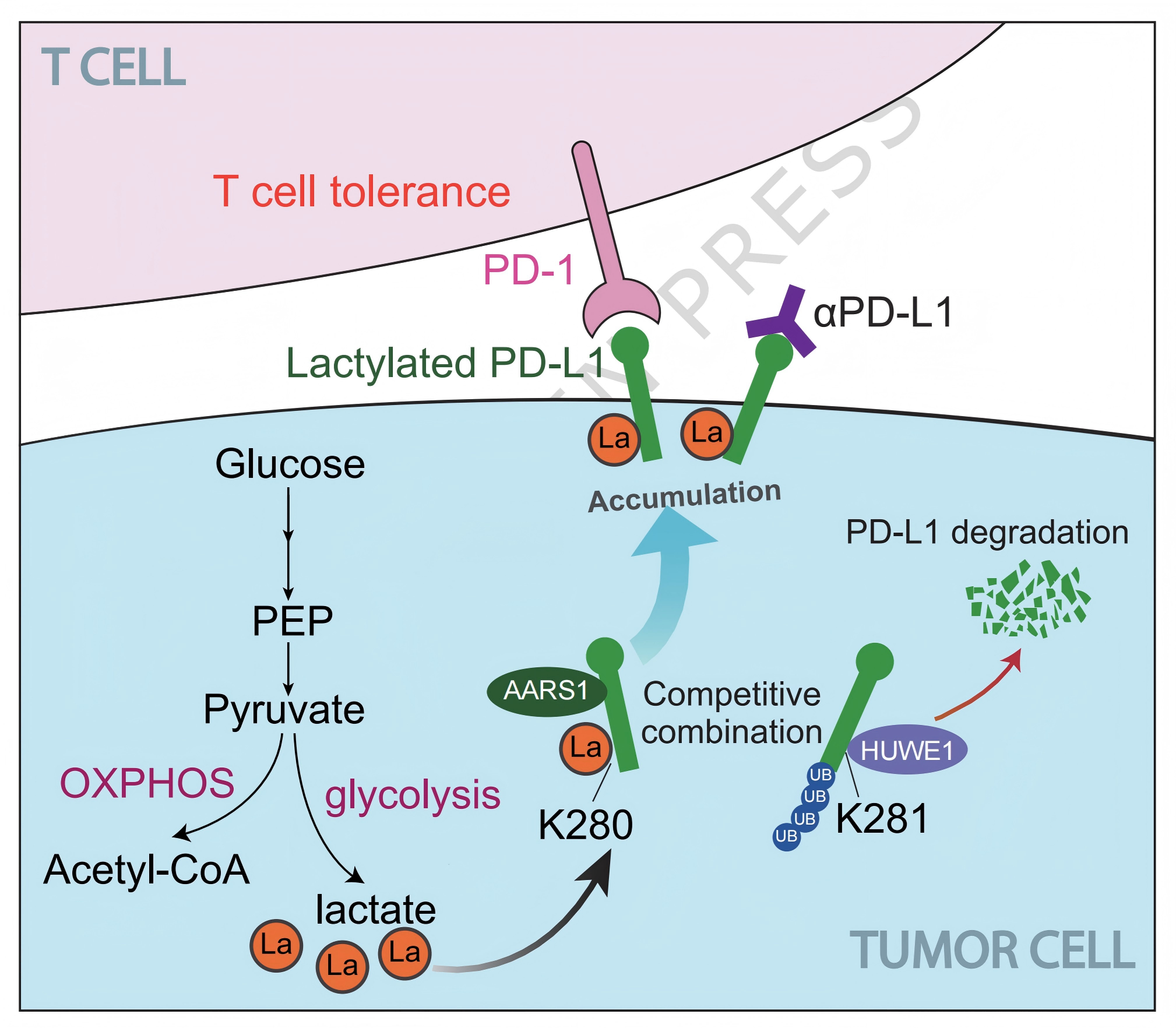
研究背景
PD-L1是肿瘤免疫逃逸的核心分子之一,其通过与T细胞表面的PD-1结合,抑制CD8+ T细胞的杀伤功能,从而帮助肿瘤逃避免疫监视。尽管PD-1/PD-L1抑制剂已广泛应用于临床,但总体响应率仍较低(约20%),提示PD-L1调控机制仍不完全清楚。
研究方法与材料
样本:
多种非小细胞肺癌细胞系(如H460、H1975、H1299)、小鼠肺癌细胞系(LLC)、乳腺癌细胞系(4T1)以及人正常支气管上皮细胞(16HBE)等;小鼠乳腺癌(4T1)和肺癌(LLC)模型;80例非小细胞肺癌患者组织样本。
方法:
1. 基因编辑:构建了PD-L1的野生型、细胞内结构域缺失突变体、不同赖氨酸位点(K)突变为精氨酸(R)的突变体等质粒,以确定关键的乳酸化位点。
2. 质谱分析:质谱鉴定PD-L1的乳酸化位点,并利用FSL-Kla工具预测潜在的乳酸化位点。
3. 细胞功能实验:T细胞杀伤实验,评估PD-L1乳酸化对肿瘤细胞抵抗免疫杀伤能力的影响。
4. 其他分子生物学实验:IP、Western blot、IHC等。
研究结果
1.乳酸上调PD-L1表达
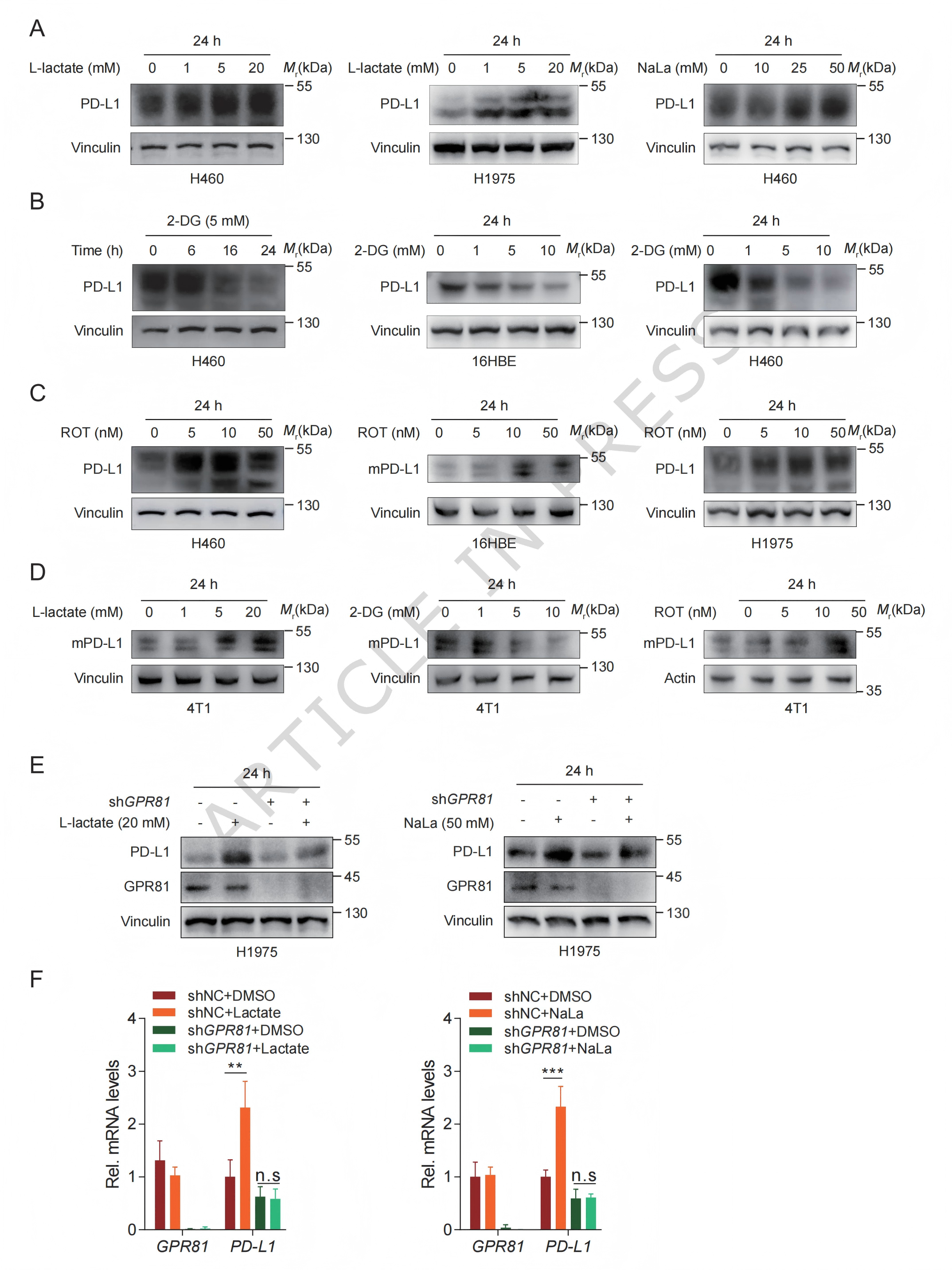
研究人员首先验证了乳酸的作用。结果如图1所示,在肺癌细胞H460和H1975中,用乳酸钠处理能剂量和时间依赖性地上调PD-L1蛋白水平 (图1A)。抑制糖酵解(减少乳酸产生)会降低PD-L1,而抑制线粒体呼吸(迫使细胞依赖糖酵解)则会上调PD-L1 (图1B, C)。先前研究表明,乳酸可通过GPR81上调PD-L1的转录。本研究也证实了这一点:敲低GPR81会降低PD-L1的mRNA和蛋白水平 (图1E, F)。但在GPR81被敲低的细胞中,乳酸依然能提升PD-L1的蛋白水平,却无法提升其mRNA水平。这暗示乳酸还存在不依赖转录的、在蛋白水平上调控PD-L1的途径。乳酸化修饰很可能就是这条途径的关键。
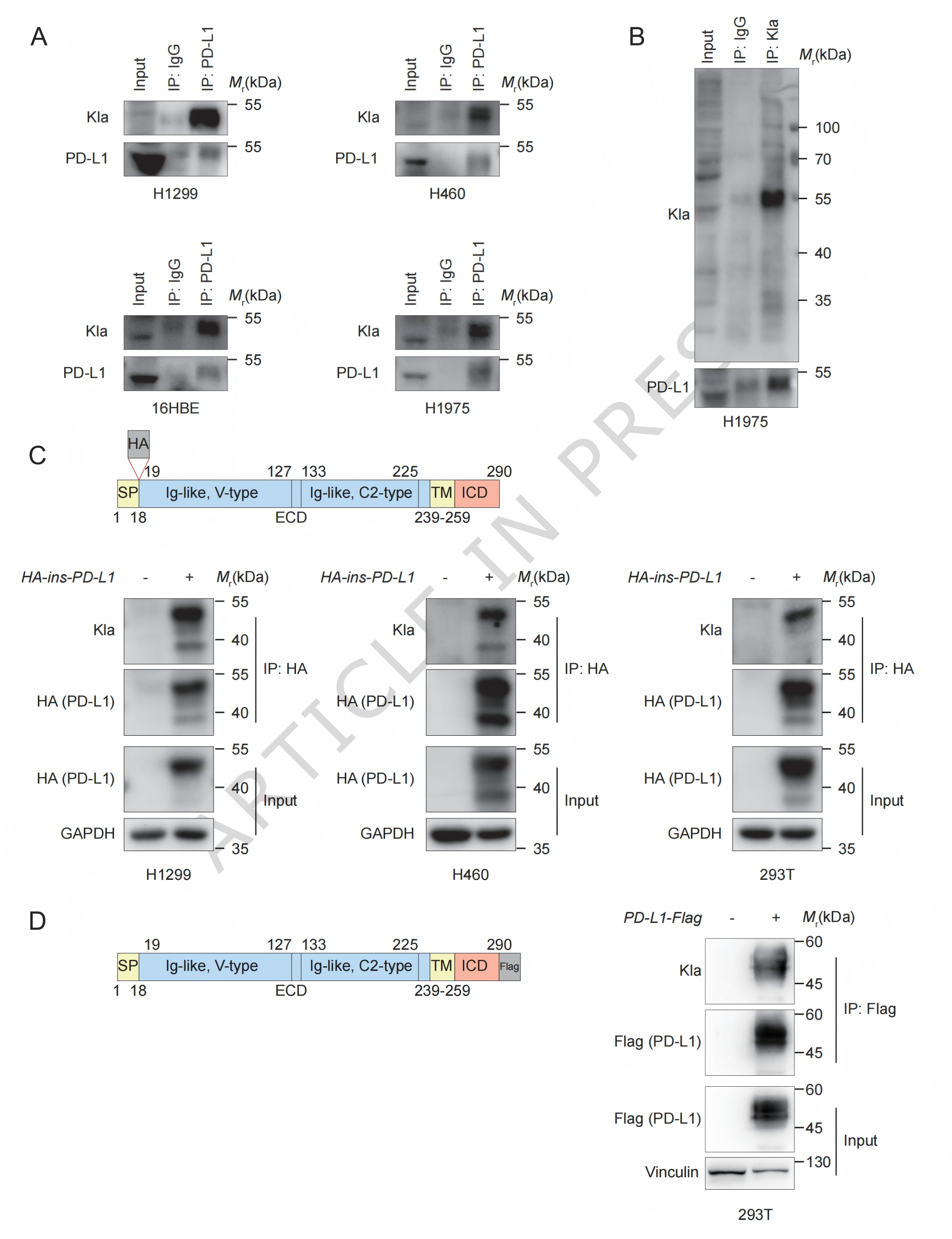
2.PD-L1存在乳酸化修饰
研究团队利用泛乳酸化修饰抗体,发现在多种细胞中都能检测到内源性PD-L1的乳酸化信号 (图2A)。进一步通过IP实验确认,PD-L1确实发生乳酸化修饰 (图2B)。他们还巧妙地构建了在信号肽后插入HA标签的PD-L1质粒,以及常规的N端Flag标签融合PD-L1质粒,通过特异性沉淀标签蛋白,均证实了PD-L1存在乳酸化修饰 (图2C, D)。这些证据链确证了PD-L1是一种乳酸化修饰蛋白。
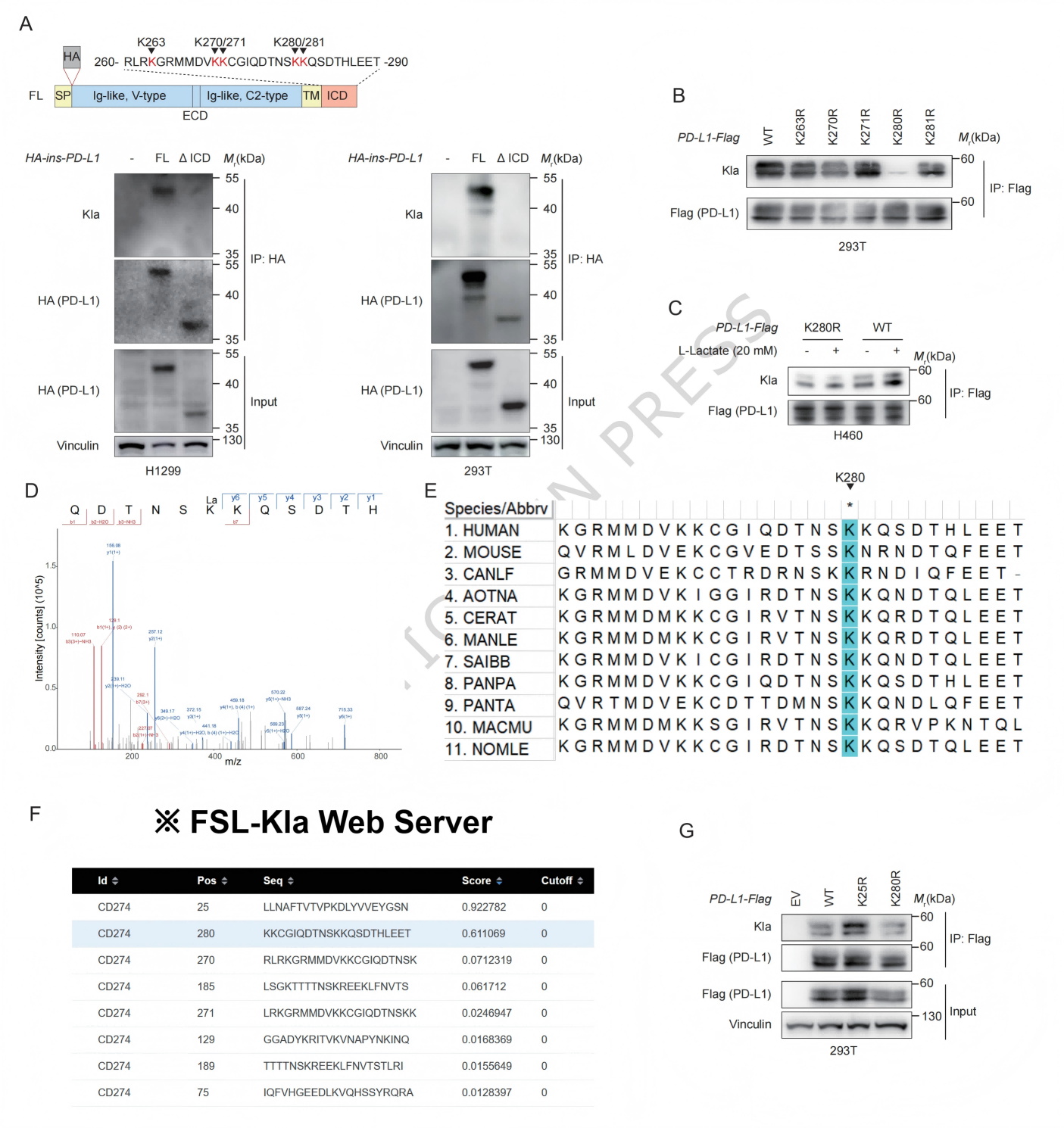
3.乳酸化位点为K280
为了找到乳酸化的具体位点,研究人员发现,删除PD-L1的细胞内结构域会几乎完全消除其乳酸化 (图3A),说明修饰位点在胞内区域。然后他们对胞内区的5个赖氨酸K逐一进行突变,发现K280R突变能几乎完全消除PD-L1的乳酸化 (图3B)。乳酸处理能显著增强野生型PD-L1的乳酸化,但对K280R突变体无效 (图3C)。质谱分析也直接鉴定到了K280位点的乳酸化肽段 (图3D)。序列比对显示,K280在不同物种中高度保守 (图3E)。利用FSL-Kla工具预测,K280是得分最高的潜在乳酸化位点之一 (图3F)。综合以上证据,K280被确定为PD-L1最主要的乳酸化修饰位点。
4.乳酸化通过抑制泛素化稳定PD-L1
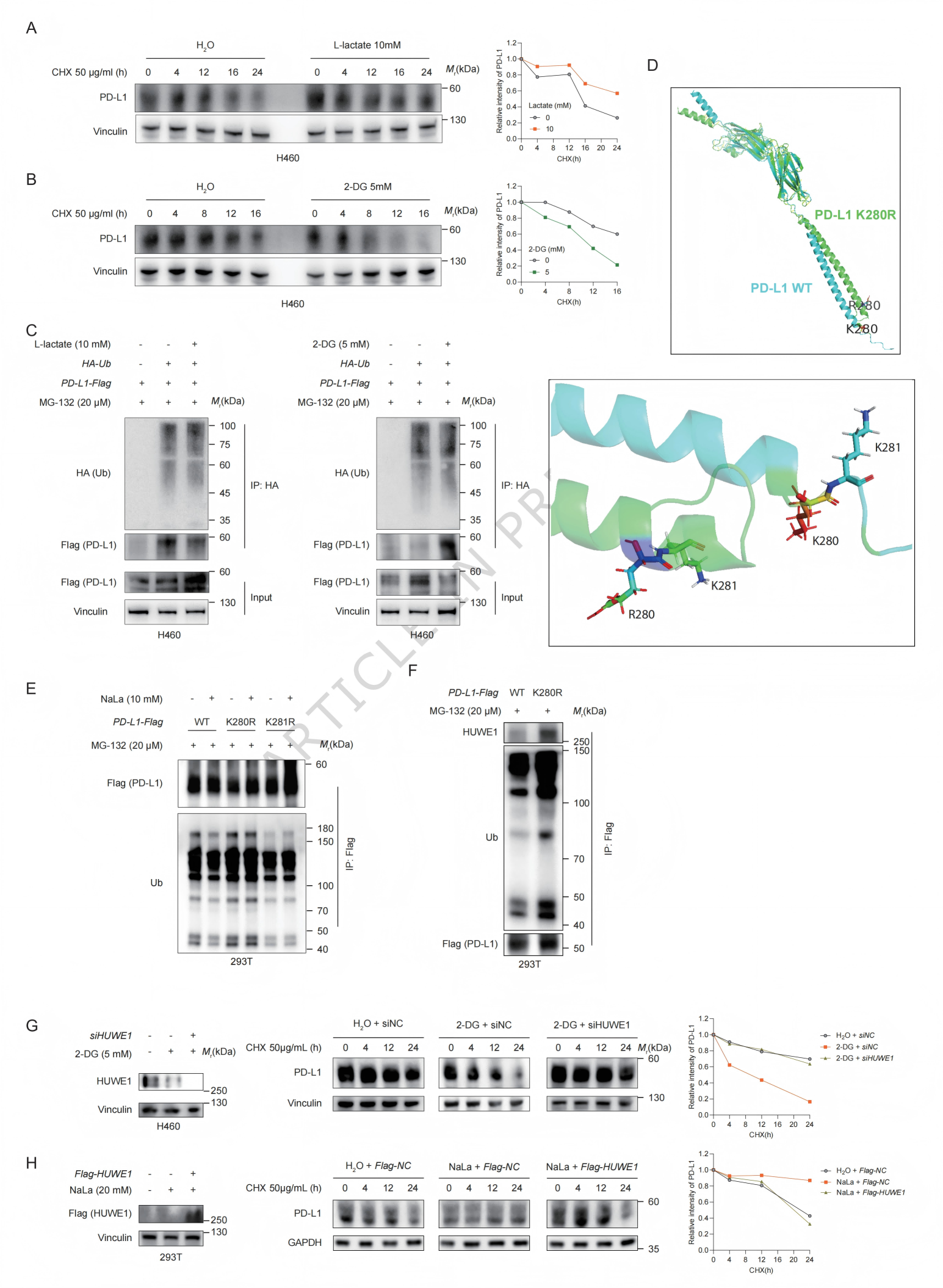
既然不是转录水平调控,那就有可能是降解调控。研究发现,乳酸处理能减缓PD-L1蛋白的降解,而抑制糖酵解则加速其降解 (图4A, B)。进一步研究发现,乳酸能抑制PD-L1的泛素化,而抑制糖酵解则增强其泛素化 (图4C)。这表明乳酸通过影响泛素化来稳定PD-L1。
关键的机制在于,K280恰好位于另一个已知泛素化位点K281旁边。文献报道,E3泛素连接酶HUWE1负责催化PD-L1的K281位点发生多聚泛素化,从而促使其被蛋白酶体降解。作者推测,K280的乳酸化可能会产生空间位阻,影响HUWE1的结合,从而保护PD-L1不被降解。实验证实,K280R突变体的泛素化水平及与HUWE1的结合能力显著强于野生型 (图4E, F)。此外,敲低HUWE1能稳定PD-L1,而过表达HUWE1则能逆转乳酸钠对PD-L1的稳定作用 (图4G, H)。这些结果证明:乳酸在K280位点的修饰,物理性地阻碍了HUWE1接近并标记PD-L1,从而阻止了其被泛素化降解。
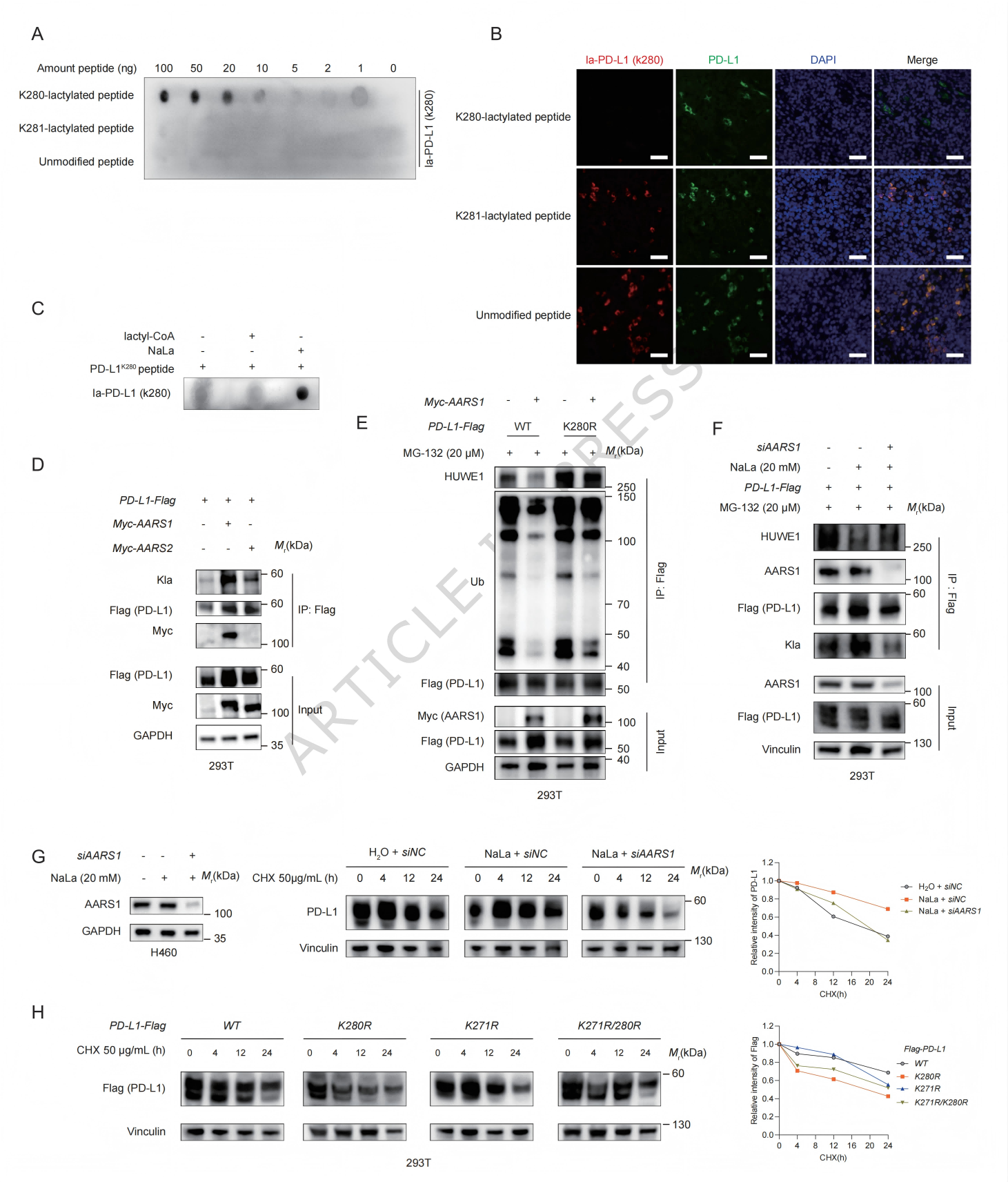
5.AARS1是关键乳酸转移酶
那么,是谁将乳酸转移到PD-L1的K280上呢?体外实验证明,乳酸本身可以直接作为供体修饰PD-L1肽段,而非其活化形式乳酰辅酶A(图5C)。细胞实验表明,氨酰-tRNA合成酶1(AARS1)能与PD-L1结合,并促进其乳酸化 (图5D)。过表达AARS1能显著降低PD-L1野生型的泛素化并破坏其与HUWE1的结合,但对K280R突变体无效 (图5E)。反之,敲低AARS1则会降低PD-L1乳酸化,增强其与HUWE1的结合,并消除乳酸钠的稳定作用 (图5F, G)。这些数据一致指向AARS1是负责催化PD-L1在K280位点发生乳酸化的关键修饰酶Writer。
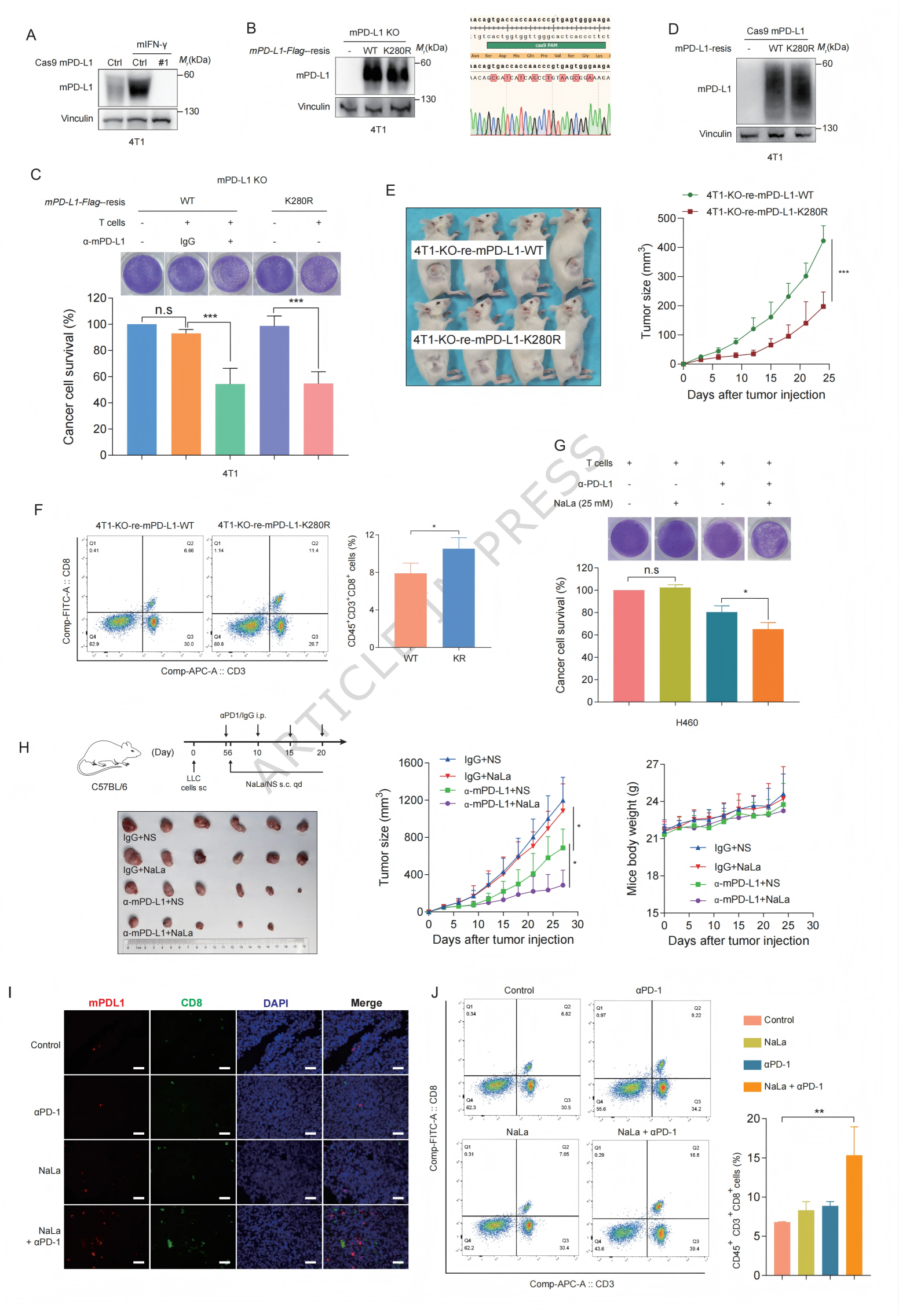
6.乳酸化促进免疫逃逸与肿瘤生长
功能实验证明,相较于表达野生型mPD-L1的小鼠乳腺癌细胞,表达K280R突变体的细胞,在T细胞杀伤实验中对CD8+ T细胞的攻击更为敏感,效果堪比使用PD-L1抗体 (图6C)。在小鼠体内成瘤实验中,表达K280R突变体的肿瘤生长显著减缓,并且肿瘤内浸润的CD8+ T细胞更多 (图6E, F)。这直接证明了K280位点的乳酸化对PD-L1的免疫抑制功能至关重要。在小鼠肺癌模型中,单独使用乳酸钠对肿瘤生长无影响,但它能显著增强抗PD-1抗体的治疗效果,且不增加明显毒性 (图6H)。多重免疫组化显示,联合治疗组肿瘤中PD-L1表达更高,同时浸润的CD8+ T细胞也更多 (图6I, J)。
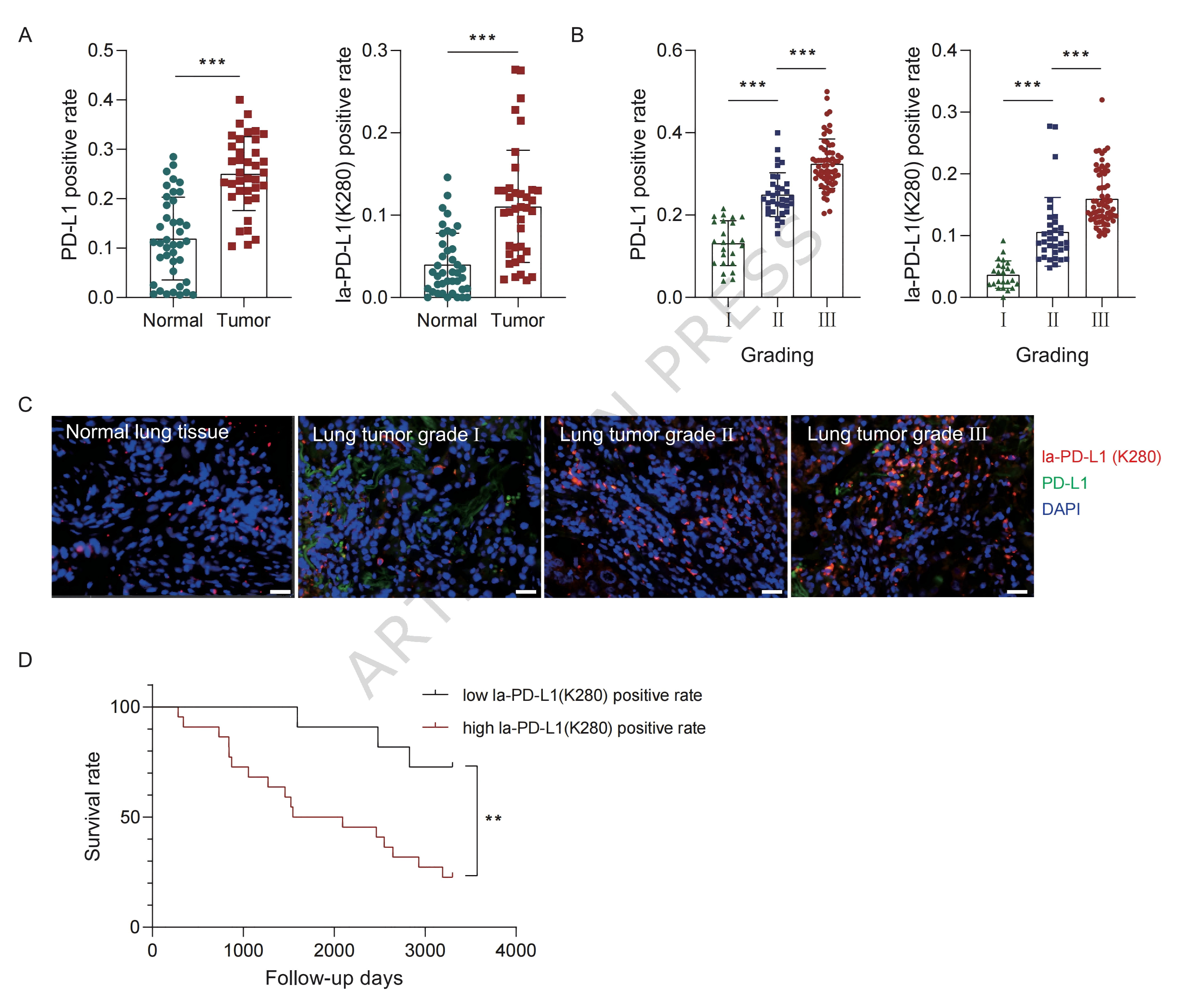
7.PD-L1乳酸化是潜在的癌症诊断生物标志物
最后,研究回归临床。利用特制的PD-L1 K280乳酸化抗体,团队分析了80例非小细胞肺癌患者组织。他们发现,肺癌组织中PD-L1乳酸化阳性率显著高于癌旁正常组织 (图7A)。更重要的是,PD-L1乳酸化水平与更晚期的肿瘤分期显著相关 (图7B)。生存分析显示,PD-L1乳酸化高表达的肺癌患者,其总生存期明显更差 (图7D)。这表明,检测PD-L1的乳酸化水平,有望成为预测患者预后和指导免疫治疗的新兴生物标志物。
总结
本研究系统性地揭示了肿瘤代谢与免疫逃逸交汇的一条全新通路,可以概括为:肿瘤细胞糖酵解产生大量乳酸 → AARS1催化PD-L1蛋白K280发生乳酸化 → 修饰阻碍E3泛素连接酶HUWE1结合而抑制PD-L1泛素化降解 → PD-L1在细胞表面异常稳定积累 → 抑制T细胞功能且促进肿瘤免疫逃逸和生长。
研究首次发现并证实了乳酸能直接修饰在蛋白上,且乳酸化修饰调控泛素化修饰,从而调控PD-L1蛋白稳定性,乳酸化PD-L1蛋白可作为潜在的诊断和预后生物标志物。
青莲百奥修饰组学解决方案
青莲百奥修饰蛋白组学产品线升级,不仅精心打磨了经典修饰产品线(如磷酸化、糖基化、泛素化等),同时开拓了一系列新型修饰产品线(如乳酸化、棕榈酰化、琥珀酰化、氧化还原等)。现凭借先进的高分辨率、高灵敏度质谱技术,积累了丰富的修饰组学研究经验,提供深入的生物信息学分析报告,为科研工作的深入探索和成果的有效转化提供强有力的支持。
