组蛋白赖氨酸甲基化的全局和局部变化在癌症进展和发展中起着关键作用,而赖氨酸特异性去甲基化酶1(LSD1,也称为KDM1A)在多种癌症中高表达,与患者不良预后显著相关。作为一种有潜力的治疗靶点,其小分子抑制剂的临床研发却受限于剂量毒性及脱靶效应,表现出较差的疾病控制效果。蛋白水解靶向嵌合体(PROTAC)技术是癌症药物发现中的全新方向,具有更高的治疗效力和耐久性,降低潜在细胞毒性,降低耐药性的可能性,并可针对不可溶蛋白等多方面优势,为靶向LSD1提供了全新的解决方案,有望突破现有疗法的限制。
近日,浙江大学孙毅、韩欣、俞卿课题组在Science Bulletin(IF 21.1)发表了题为“LD-110, a potent LSD1 PROTAC degrader, suppresses tumor growth by inducing ER stress and apoptosis”的研究论文,该研究设计并合成了靶向LSD1的强效PROTAC降解剂LD-110,能够通过激活ATF4-CHOP信号触发内质网应激,导致NOXA上调和MCL1下调,最终诱导细胞凋亡。LD-110在乳腺和肺部异种肿瘤模型中表现出良好的体内药物动力学特征,并有效抑制体内肿瘤生长。本文开发了一种针对LSD1且具有有效抗癌活性的强效PROTAC降解剂,未来有望成为潜在的抗癌药物。
北京青莲百奥生物科技有限公司为文章提供了转录组学服务。

重要成果
一、LD-110是一种针对LSD1的高效PROTAC降解剂
为筛选构建PROTAC的最佳LSD1靶向弹头,研究比较了已报道抑制剂LI-1与两个临床阶段候选药物ORY-1001和GSK2879552在肺癌细胞系中的生长抑制效果。结果显示,LI-1对两种细胞系均呈现剂量依赖性生长抑制。随后,研究团队以LI-1为弹头、沙利度胺为CRBN结合配体,合成了一系列PROTAC降解剂。经Western blot系统筛选LSD1降解效率,最终鉴定出LD-110为最优化合物,并将其作为本研究的先导化合物进行全面生物学评价。
在乳腺癌细胞中,LD-110处理可诱导LSD1蛋白呈时间和剂量依赖性降解,同时伴随其下游标志物H3K4me2水平升高。其对肺癌细胞系也具有降解活性,效果略低于乳腺癌细胞。平行比较显示,LD-110可显著提高H3K4me2水平,提示其通过降解作用更有效地抑制了LSD1的去甲基化酶活性。结果表明,LD-110是一种高效PROTAC LSD1降解剂,通过催化降解而非酶抑制机制,相较于其弹头分子LI-1表现出显著增强的LSD1抑制活性。
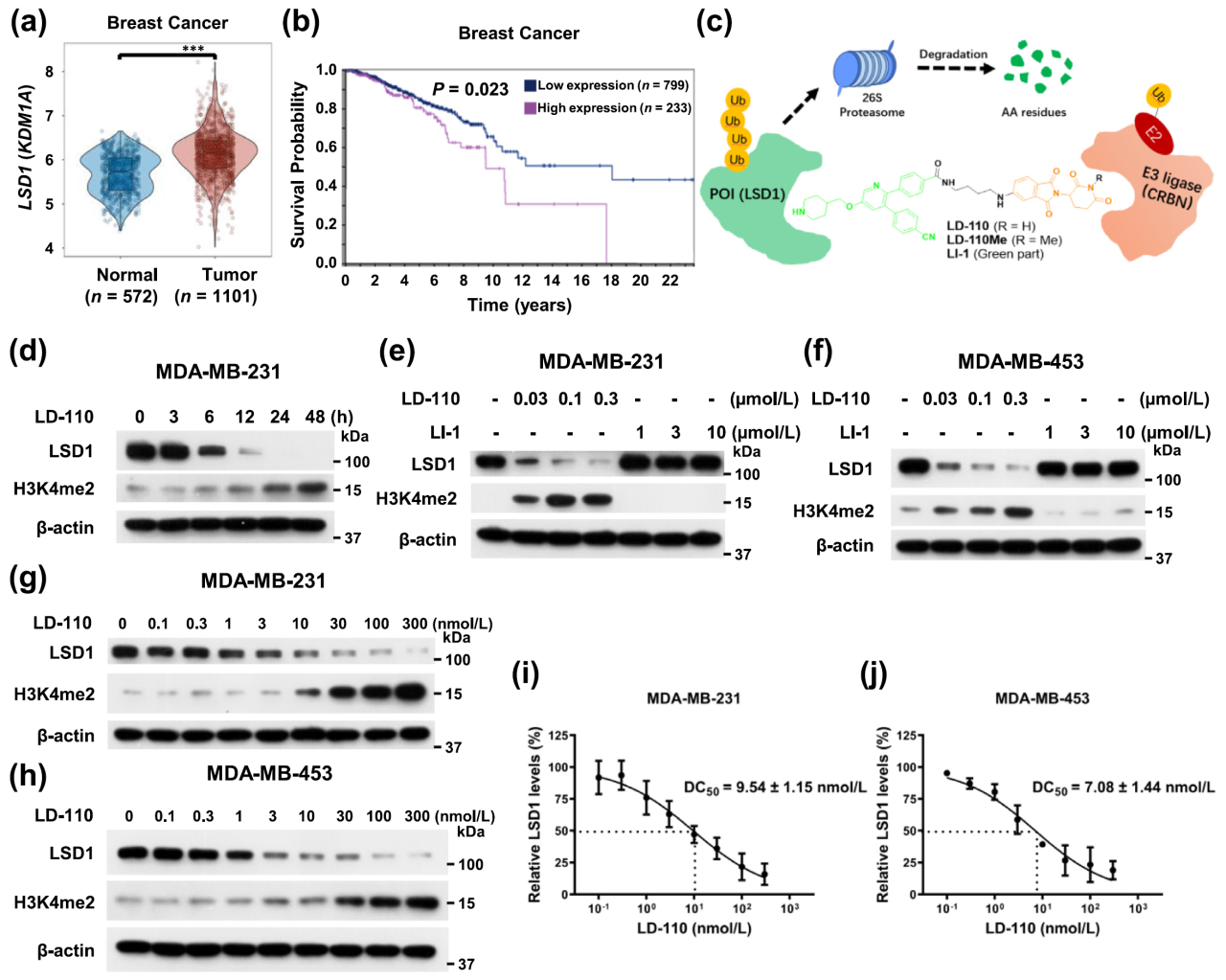
图1. LD-110是一种针对LSD1的高效PROTAC降解剂
二、LD-110通过UPS降解LSD1
机制研究表明,使用LI-1或沙利度胺阻断LSD1-CRBN互作可有效抑制LD-110介导的LSD1降解;而neddylation抑制剂MLN4924或蛋白酶体抑制剂MG132预处理同样能阻断该降解过程。为验证LD-110的靶向特异性,研究设计合成了无法结合CRBN的结构类似物LD-110Me,结果发现即使在72小时处理下,LD-110Me既不能降解LSD1,也无法引起H3K4me2积累。此外也排除了LD-110、LI-1或LD-110Me在相关细胞系中调控LSD1 mRNA水平的可能性。
通过质谱分析LD-110对MDA-MB-231细胞全蛋白质组的影响,发现其选择性降低LSD1与GSPT1蛋白丰度,对其他蛋白无明显影响。LD-110特异性降解LSD1及CRBN新底物GSPT1,但不影响LSD1-CoREST-HDAC1/2复合物其他组分,此外还发现LD-110对LSD1和GSPT1的降解呈时间依赖模式。上述结果从机制上证实,LD-110通过泛素-蛋白酶体系统介导的降解途径选择性清除LSD1,并协同下调GSPT1。
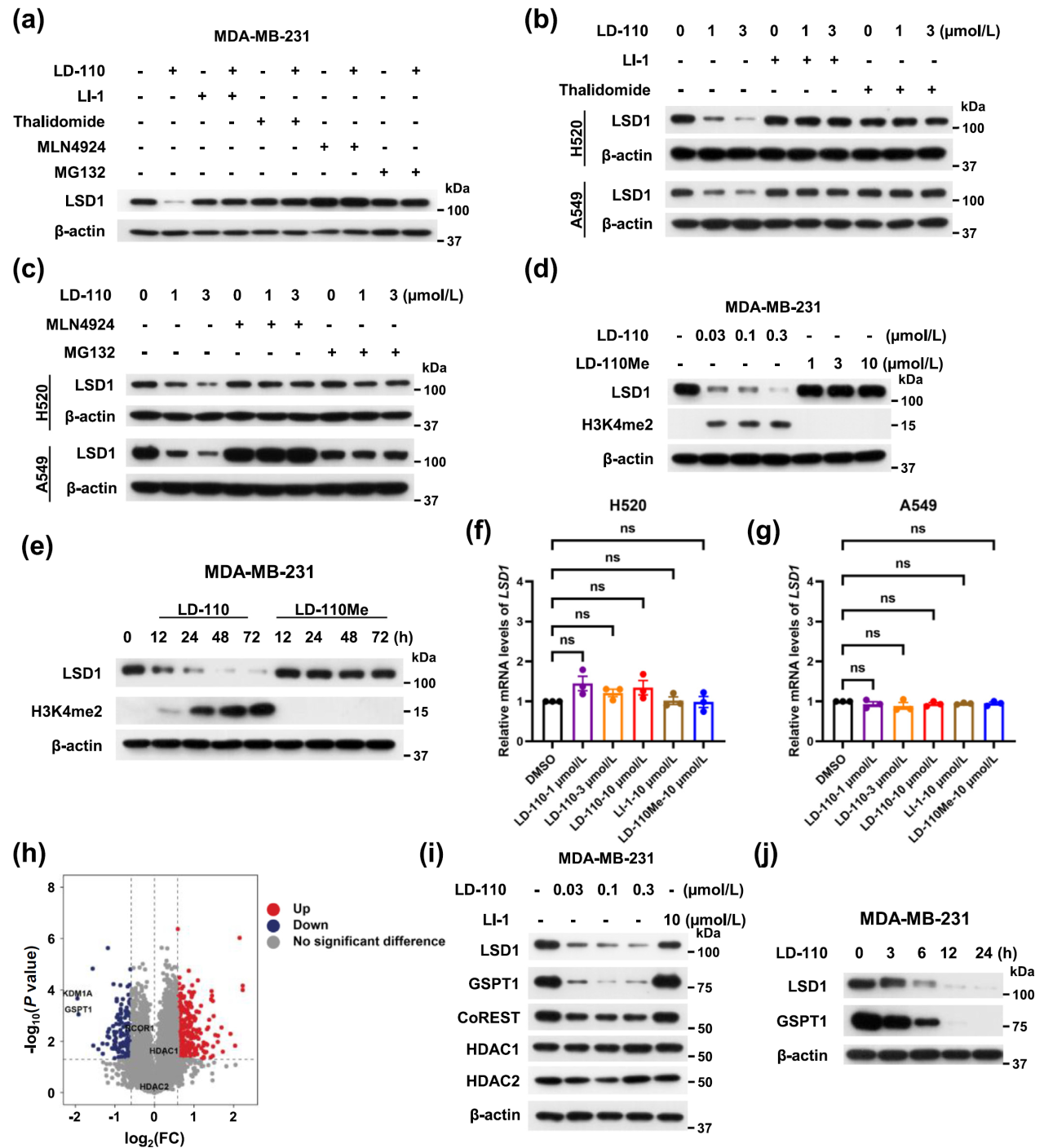
图2. LD-110通过泛素-蛋白酶体途径促进LSD1降解
三、LD-110显著抑制癌细胞的生长和存活
随后,研究进一步评估了LD-110的生长抑制活性,发现LD-110在乳腺癌细胞中呈现显著的剂量依赖性生长抑制,在肺癌细胞中同样表现出较强的抑制效果抑制效果。为明确LD-110抑制细胞生长的主要靶点,研究分别敲低LSD1或GSPT1表达。结果显示,敲低LSD1的细胞对LD-110的敏感性下降3-10倍,而敲低GSPT1能增强细胞对LD-110的敏感性且并未引起H3K4me2水平升高。单独敲低LSD1或GSPT1均可抑制细胞生长,而同时敲低两者则产生更强的生长抑制效应。除细胞毒性检测外,研究还通过克隆形成实验评估LD-110对癌细胞集落形成能力的影响,发现LD-110在乳腺癌细胞及肺癌细胞系中均呈现剂量依赖性集落形成抑制。因此,LD-110通过降解LSD1在抑制乳腺癌和肺癌细胞增殖与存活方面展现出优越的治疗潜力。
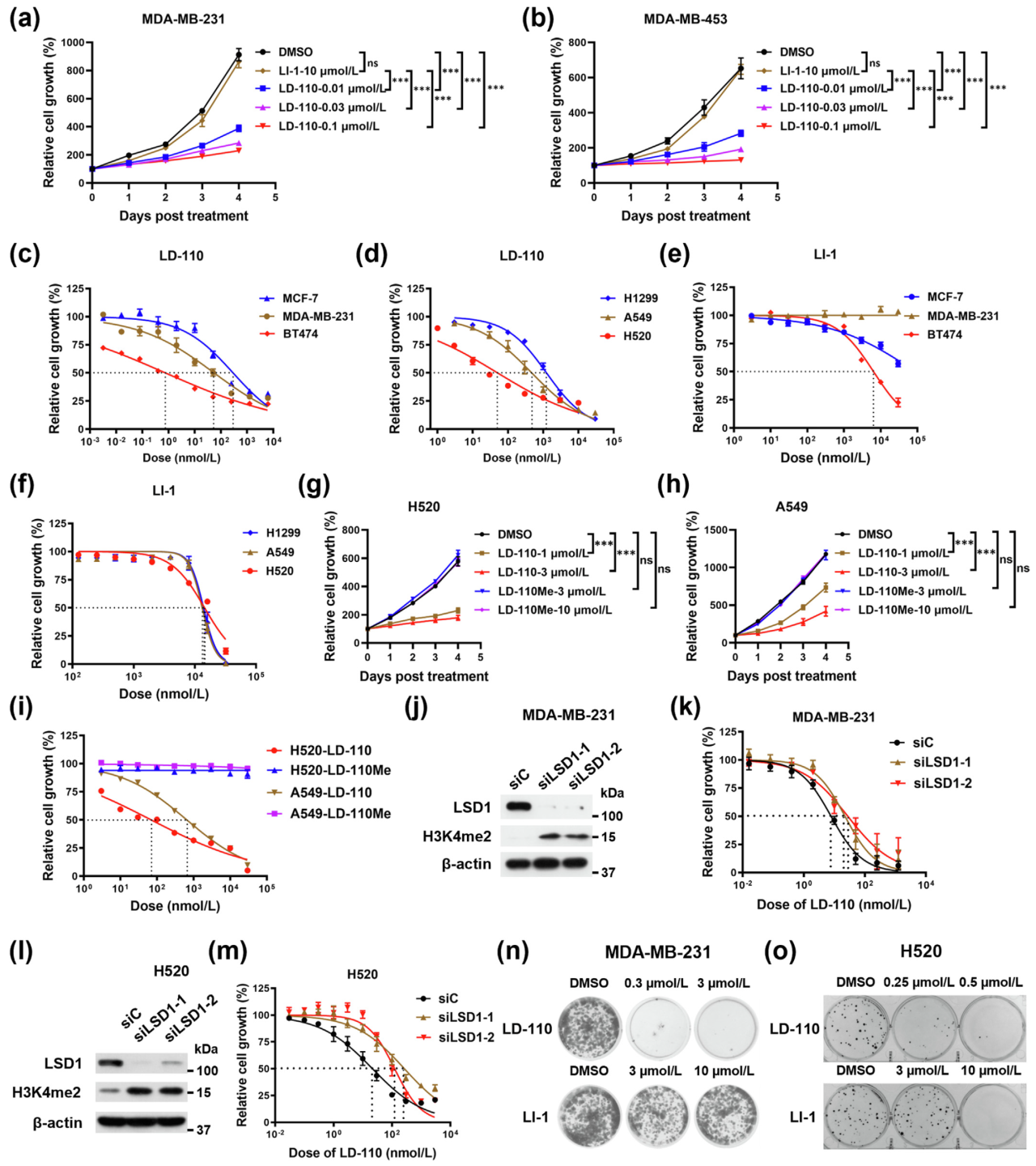
图3. LD-110显著抑制癌细胞的生长和存活
四、LD-110上调与内质网应激相关基因的表达
为了阐明LD-110抑制癌细胞生长与存活的内在机制,研究对三组独立的LD-110处理组与未处理组进行了RNA-seq分析。GO富集分析显示,显著激活的通路主要集中于内质网应激、细胞凋亡及DNA损伤相关途径。随后研究聚焦于内质网应激通路相关基因,发现内质网未折叠蛋白反应通路相关基因均存在显著富集,qRT-PCR也验证了多个内质网应激相关基因(包括ATF4、ATF3、CHOP和TRIB3)的转录水平显著上调。接下来,研究检测了ATF4和CHOP的蛋白水平,证实LD-110处理后的细胞中这两种蛋白含量均显著增加,敲低LSD1也会引起ATF4和CHOP蛋白水平升高。研究结果明确表明:LD-110通过降解LSD1,在表观遗传层面上调内质网应激相关基因,并激活ATF4-CHOP信号转导级联通路。
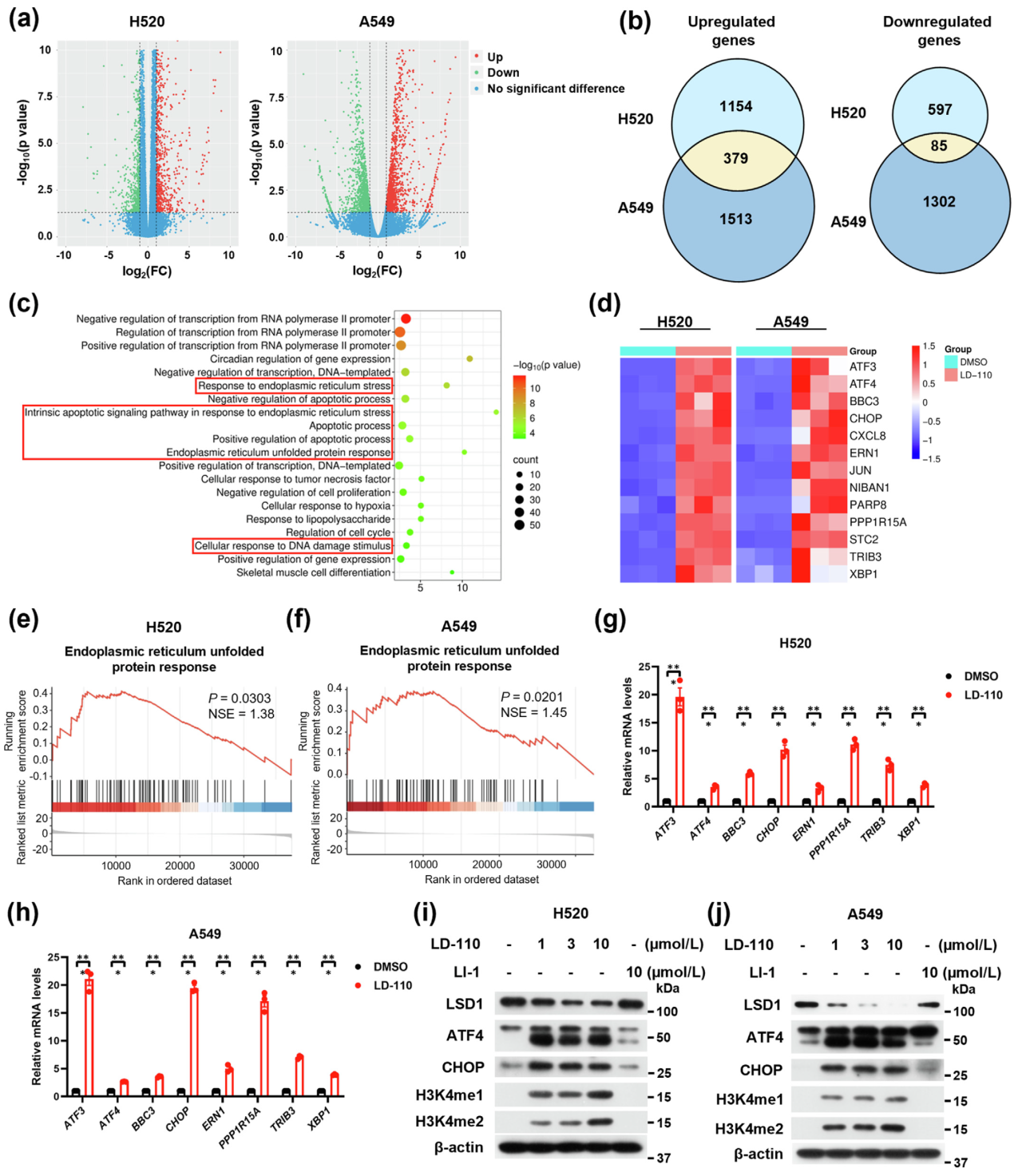
图4. LD-110表观遗传上调与内质网应激相关基因的表达
五、LD-110通过激活ATF4-CHOP-NOXA-MCL1轴来诱导细胞凋亡
RNA-seq分析同时显示,LD-110处理能显著上调细胞凋亡相关通路,与既往研究中LSD1抑制剂在白血病细胞系中引发凋亡的发现相符。流式细胞术分析表明,LD-110能剂量依赖性地诱导肺癌、乳腺癌细胞凋亡,其处理显著增加了剪切PARP与caspase 3这两种公认的凋亡标志蛋白的表达水平。
GO分析与GSEA分析均显示,细胞中响应内质网应激的内源性凋亡信号通路相关基因显著上调。使用内质网应激抑制剂牛磺熊去氧胆酸(TUDCA)处理,能显著减弱LD-110在细胞中诱导的凋亡。进一步研究发现,LD-110通过降解LSD1,上调促凋亡蛋白NOXA的水平,同时下调抗凋亡蛋白MCL1的水平,这两种蛋白均为ATF4-CHOP信号通路的下游组分。此外,TUDCA能显著逆转LD-110诱导的NOXA上调和MCL1下调,表明内质网应激位于NOXA与MCL1的上游。生物学功能实验也证实TUDCA有效缓解了LD-110对肺癌细胞活力的抑制作用。上述研究结果表明,LD-110通过激活ATF4-CHOP-NOXA-MCL1信号轴触发细胞凋亡。
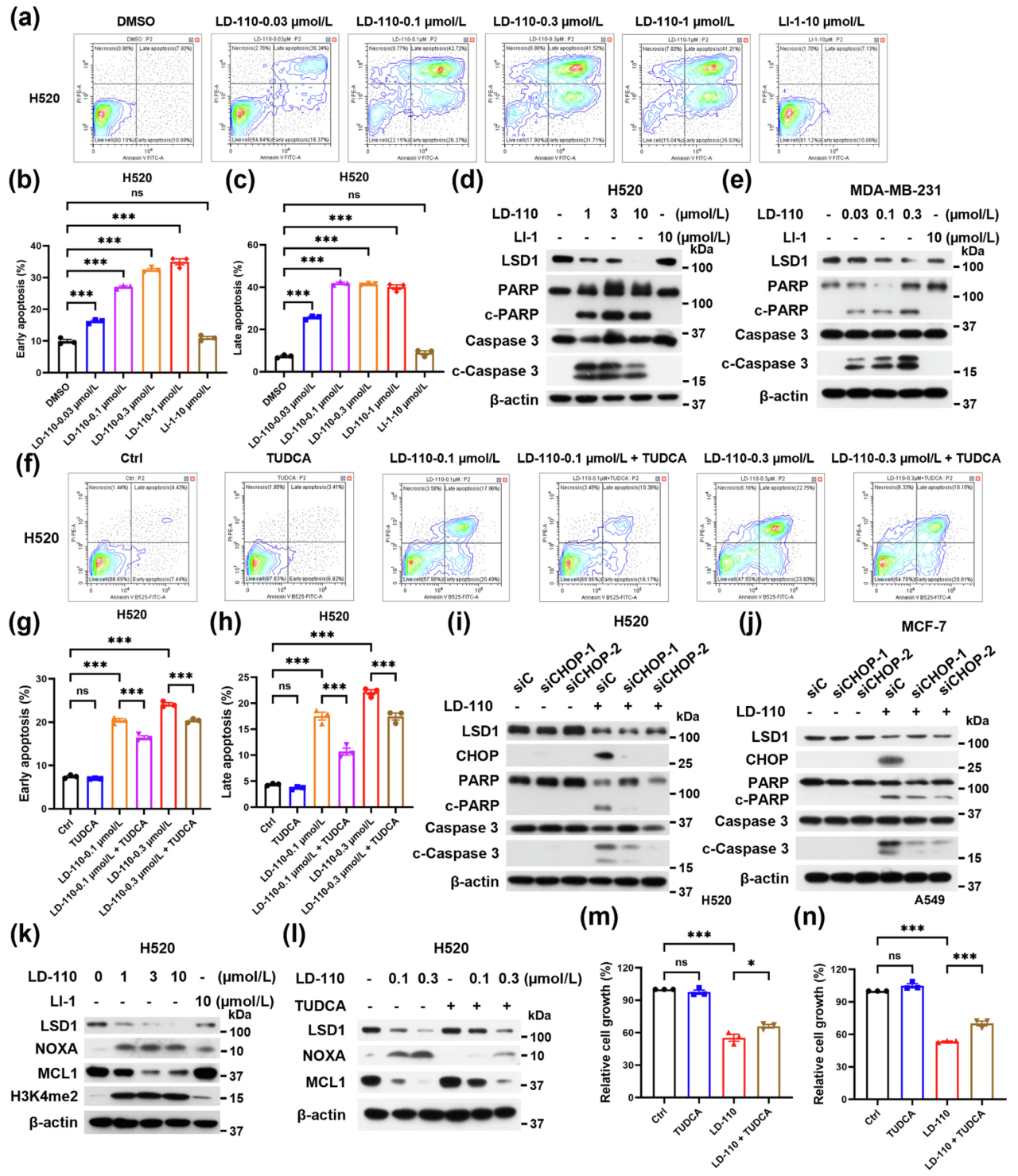
图5. LD-110通过激活ATF4-CHOP-NOXA-MCL1轴来诱导细胞凋亡
六、LD-110诱导的凋亡可归因于ROS引起的DNA损伤
RNA-seq分析还显示,LD-110处理能上调肺癌细胞中DNA损伤响应相关基因的表达,基于这一线索进行后续研究,发现LD-110确实能显著诱导γ-H2AX的剂量依赖性积累。免疫荧光分析进一步证实,经LD-110处理的细胞中γ-H2AX焦点显著形成,且在撤除LD-110长达24小时后信号仍持续存在,表明DNA损伤已无法修复。
活性氧(ROS)是DNA损伤的重要介质,LD-110处理能显著提升细胞中的ROS水平。使用抗氧化剂N-乙酰半胱氨酸(NAC)清除ROS,可部分逆转LD-110在H520细胞中诱导的凋亡,并缓解其对H520和A549细胞生长的抑制,这证明了ROS在此过程中的关键作用。随后的WB实验发现,LD-110能有效激活GCN2并诱导eIF2α磷酸化,eIF2α的持续激活与细胞毒性及凋亡相关,这一过程可通过增强ATF4的翻译来促进。综上所述,ROS的诱导生成及DNA损伤共同促进了LD-110在肺癌细胞中诱导的凋亡表型。
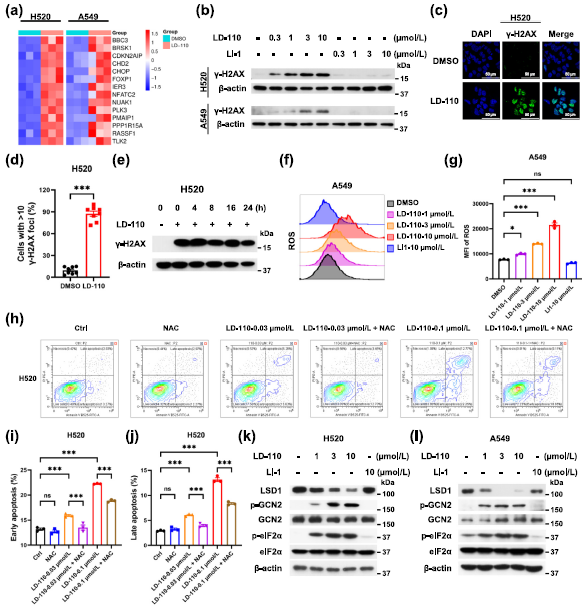 图6. LD-110诱导的凋亡可归因于ROS引起的DNA损伤
图6. LD-110诱导的凋亡可归因于ROS引起的DNA损伤
七、LD-110在体内有效抑制肿瘤生长
基于我们发现具有临床开发潜力的新型PROTAC类LSD1降解剂的目标,研究评估了LD-110在小鼠体内静脉注射与腹腔给药的药代动力学(Pharmacokinetics,PK)特征。PK数据显示LD-110整体药代动力学性质(清除率、分布容积、半衰期)良好。随后研究通过细胞来源的异种移植瘤模型评估了LD-110的体内抗肿瘤活性,发现在异种移植瘤模型中,LD-110能有效抑制肿瘤生长,表现为肿瘤生长速率、体积及重量的显著降低。IHC染色显示,LD-110处理显著降低了肿瘤组织中LSD1与Ki67的表达水平。此外LD-110给药未表现出明显的小鼠毒性迹象。WB分析显示,LD-110处理能降低LSD1与MCL1蛋白水平,同时上调ATF4-CHOP-NOXA信号轴相关蛋白表达,证实LD-110确实能在体内肿瘤组织中调节靶点活性。因此,LD-110作为一种具有前景的PROTAC类LSD1降解剂,能够有效抑制体内肿瘤生长。
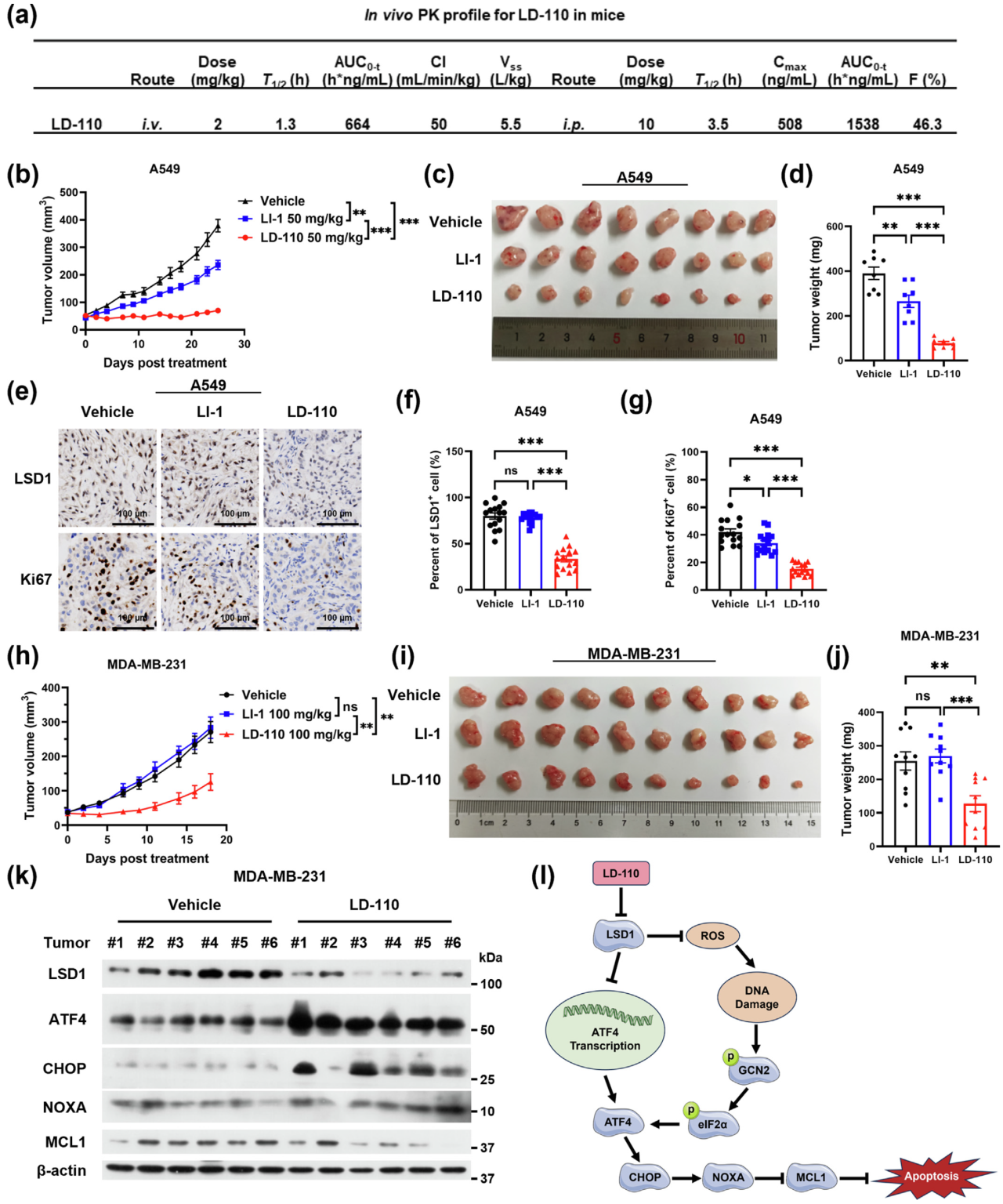
图7. LD-110在体内有效抑制肿瘤生长
文章结论
本研究开发了一种新型高效的PROTAC类LSD1降解剂——LD-110。该化合物在体外细胞系和体内异种移植瘤模型中,均展现出对肺癌和乳腺癌显著的生长抑制活性,并具备良好的药代动力学特性。
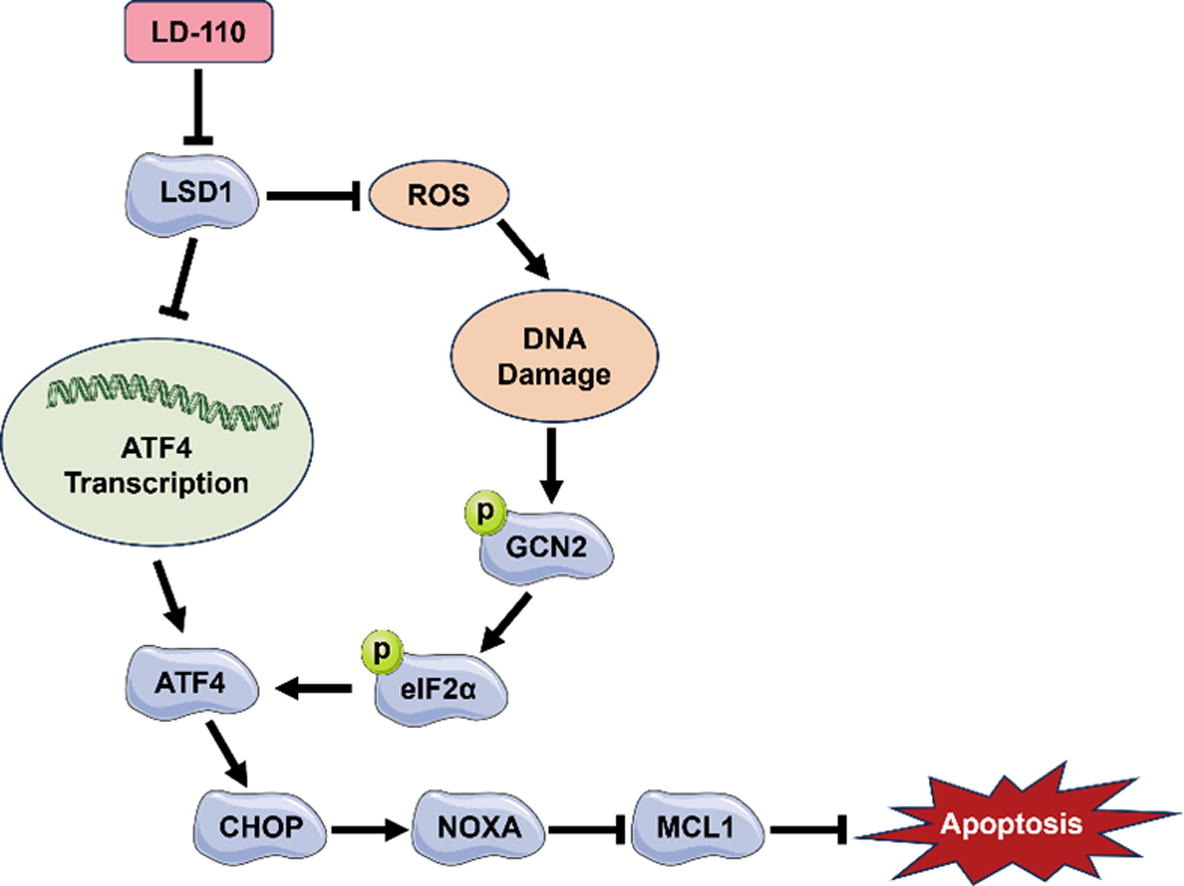
从作用机制角度,本研究构建了以下工作模型:LD-110通过降解LSD1,一方面触发内质网应激以增强ATF4转录,另一方面通过增加ROS生成和DNA损伤激活GCN2-eIF2α信号轴,从而促进ATF4蛋白翻译。这两条通路的协同作用最终导致CHOP表达上调,进而引起NOXA水平升高与MCL1水平降低,最终诱导肿瘤细胞凋亡。LD-110的发现为未来开发通过靶向降解LSD1的新型抗癌药物奠定了坚实基础。
参考文献
Zhai D, Zhuo J, Yin Y, Li L, Liang M, Zhou X, Liu L, Chen L, Xiong X, Yu Q, Han X, Sun Y. LD-110, a potent LSD1 PROTAC degrader, suppresses tumor growth by inducing ER stress and apoptosis. Sci Bull (Beijing). 2025 Oct 21:S2095-9273(25)01046-1.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
