前列腺癌(Prostate Cancer,PCa)是全球男性第二大高发恶性肿瘤,其发病率和死亡率持续攀升,每年导致数十万患者死亡。尤其是当癌症发展到晚期转移阶段,患者预后将显著恶化。尽管以PD-1/PD-L1抑制剂为代表的免疫检查点疗法在多种恶性肿瘤治疗中取得显著成效,其针对免疫"冷肿瘤"特性的PCa却收效甚微。这类肿瘤具有独特的免疫逃逸能力,能够有效躲避机体免疫监视,具体机制至今仍是肿瘤免疫治疗领域亟待攻克的重要科学难题。
最近,浙江大学医学院附属邵逸夫医院陈艺成/丁国庆/余燕岚/张杰团队于Cancer Res(IF=16.6)杂志上发表了题为“Prostate Cancer Cells Secrete PD-1 in Exosomes to Enhance Myeloid-Derived Suppressor Cell Activity and Promote Tumor Immune Evasion”的研究论文。该研究基于临床队列统计分析和动物、细胞模型的组学分析,发现原本应该出现在免疫细胞上的PD-1分子在前列腺癌细胞上也有表达,并与预后不良高度相关。因此进一步探索肿瘤细胞内源性PD-1表达在免疫逃逸方向的机制作用,为前列腺癌免疫治疗方案提供了新的思路。
北京青莲百奥生物科技有限公司为该研究提供了蛋白质组学检测服务。
 研究结果
研究结果
一、PCa中PD-1与肿瘤的恶性程度呈正相关
研究采用qPCR和WB检测了正常前列腺上皮细胞系RWPE-1及多种PCa细胞系中PD-1的mRNA和蛋白表达水平。结果显示,与正常前列腺上皮细胞相比,PCa细胞中的PD-1表达显著上调。通过双免疫荧光标记发现,肿瘤组织内存在内源性PD-1表达,仅在浸润的免疫细胞中观察到少量共定位现象。随后的流式分析也同样显示,在上皮细胞黏附分子(EpCAM)标记的PCa上皮细胞中可检测到PD-1阳性表达。
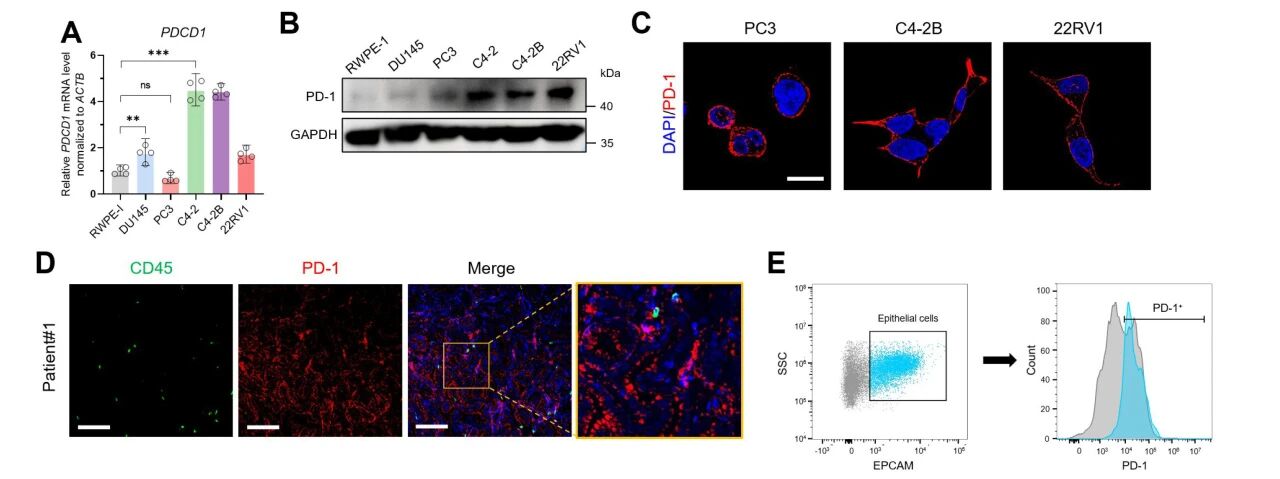
临床分析中,研究团队对近百例前列腺癌临床样本进行统计,并计算其Gleason评分。通过qPCR和IHC分别检测基因和蛋白表达水平,发现肿瘤恶性程度与癌细胞PD-1表达水平呈显著正相关。
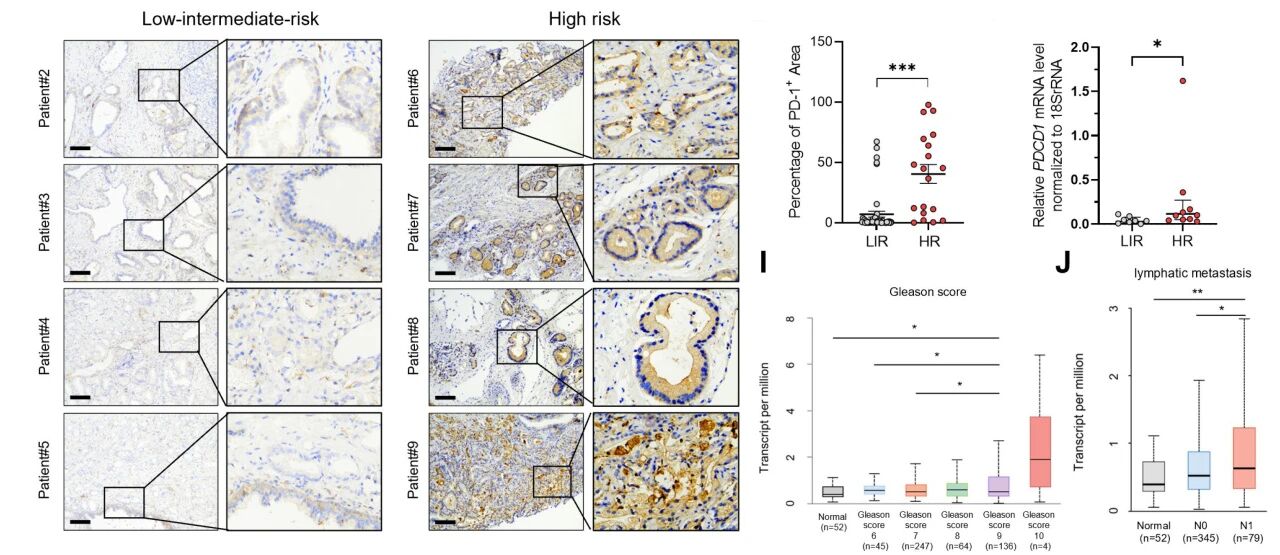
二、PD-1在PCa中通过调节免疫途径促进肿瘤生长
为了探究内源性PD-1对PCa肿瘤生长的影响,研究通过CRISPR-Cas9在RM-1 PCa细胞中构建了Pdcd1敲除细胞模型。检测显示,Pdcd1缺失并未显著影响细胞增殖能力,但将Pdcd1敲除的PCa细胞皮下接种至野生型C57BL/6J小鼠体内时,发现其体内生长受到显著抑制。相比之下,过表达PD-1的PCa细胞在小鼠体内呈现快速生长趋势,而体外增殖也未受影响。
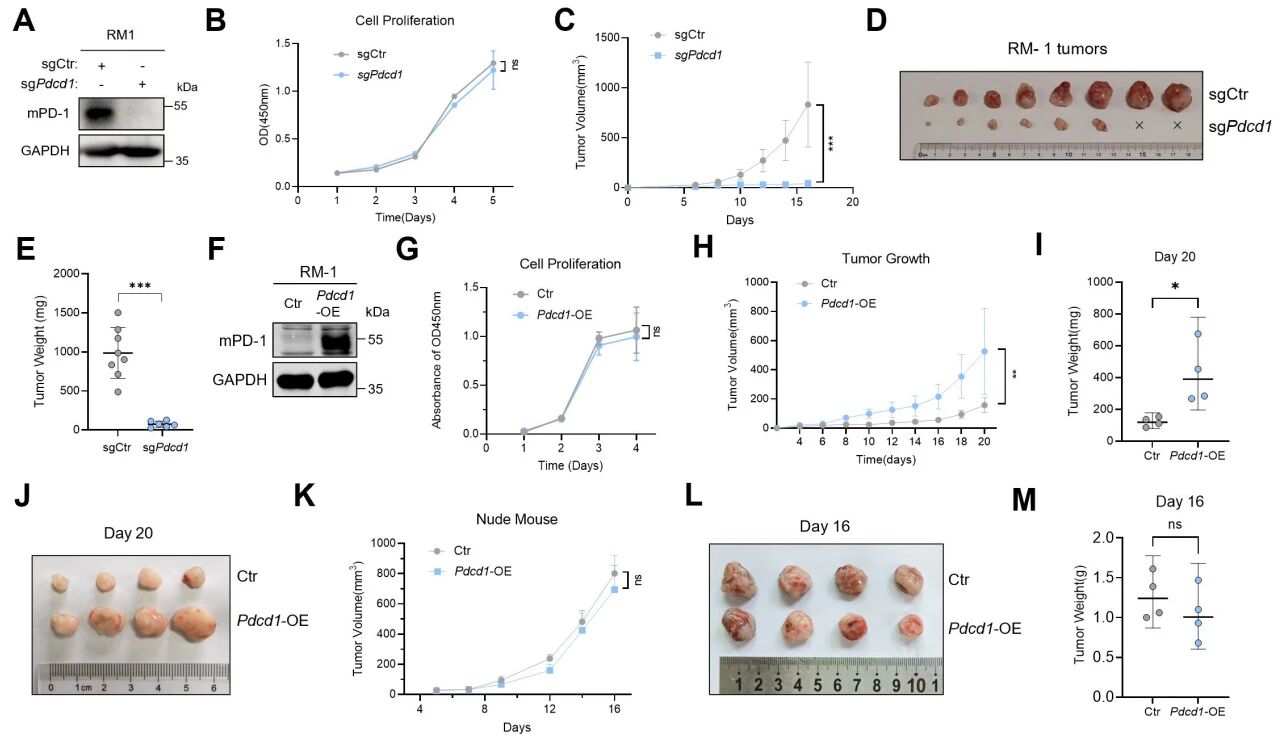
进一步观察发现,内源性PD-1的促肿瘤效应与其T细胞免疫功能密切相关,肿瘤组织的免疫荧光染色也显示,在肿瘤细胞中的PD-1过表达会导致CD8+ T细胞浸润显著减少。因此研究认为,PCa中的内源性PD-1可能通过调控CD8+ T细胞的浸润来影响肿瘤生长,这种免疫调节作用可能普遍存在于多种肿瘤类型中。
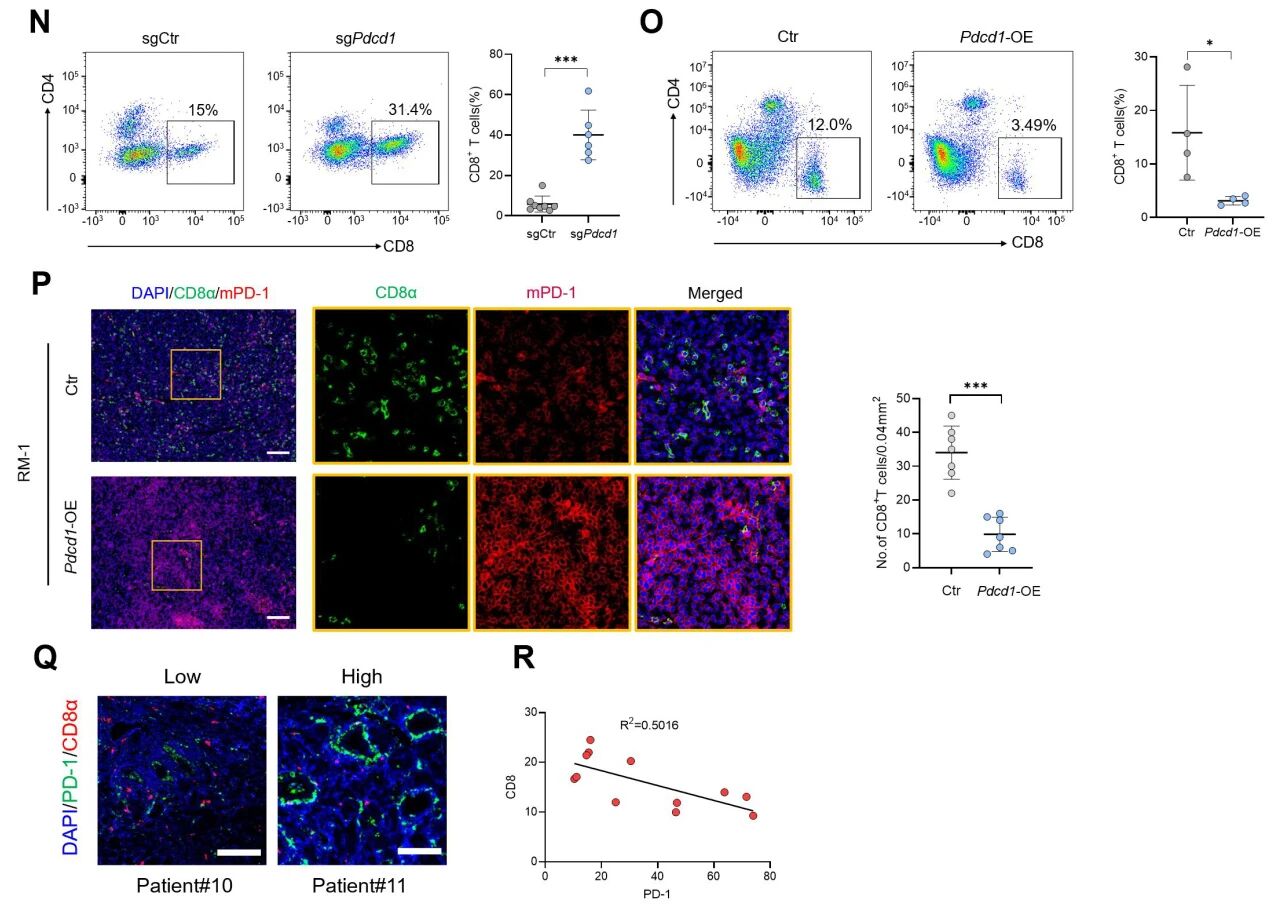
三、MDSCs在肿瘤内源性PD-1介导的免疫抑制中发挥关键作用
为了探究肿瘤中内源性PD-1介导的免疫调节机制,研究对小鼠皮下移植PCa模型进行了全面的单细胞测序分析。结果表明,PD-1介导的免疫抑制可能涉及多种细胞类型,包括骨髓来源的抑制性细胞(MDSCs)、单核细胞、CD8+ T细胞和自然杀伤(NK)细胞。其中最显著的变化出现在MDSCs和CD8+ T细胞中,这一结果也通过流式分析证实。PMN-MDSCs被广泛认为是病理激活中性粒细胞的一个亚群,具有出强大的免疫抑制活性,并通过抑制CD8+ T细胞和NK细胞介导的免疫应答来促进肿瘤进展。因此,研究推测CD8+ T细胞和PMN-MDSCs可能是肿瘤内PD-1效应的潜在靶细胞。
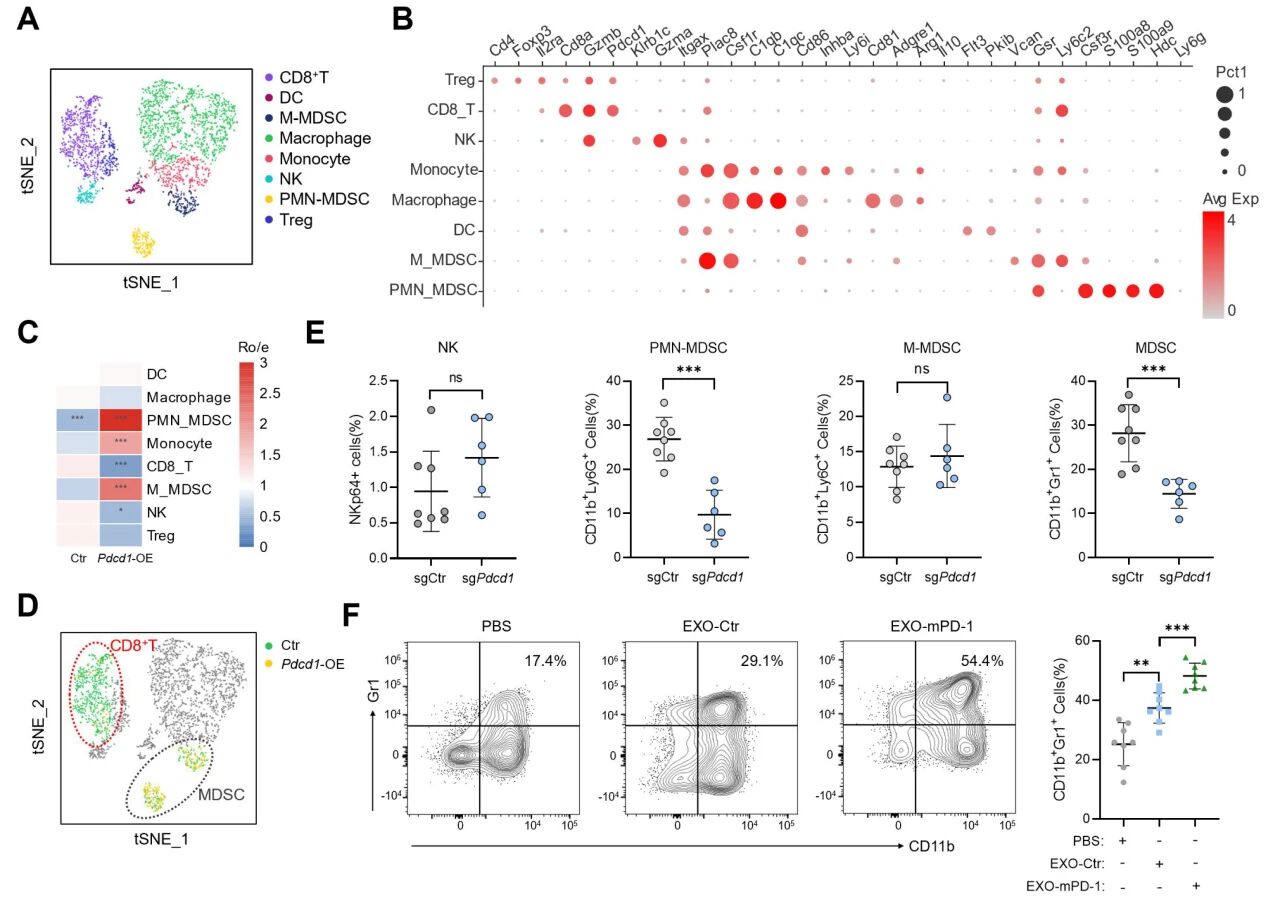
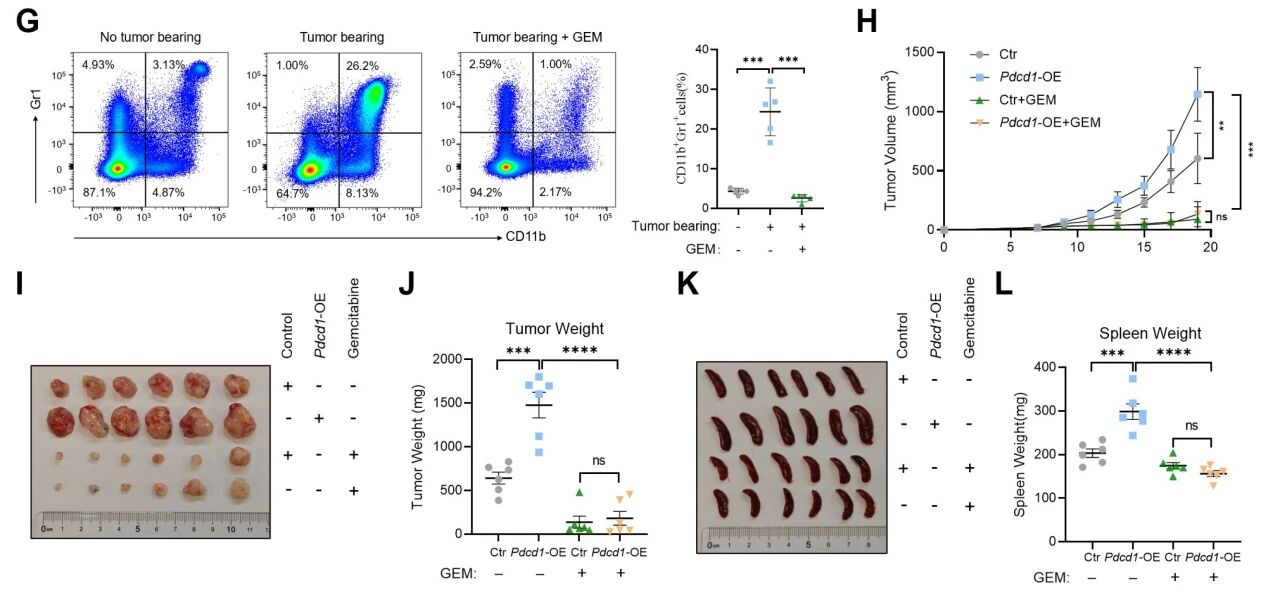
为阐明MDSCs在PD-1介导的免疫抑制中的潜在作用,研究建立了小鼠模型,通过化疗药物吉西他滨(GEM)清除MDSCs,发现其消除了内源性PD-1在前列腺癌中诱导的促肿瘤效应。此外,清除MDSCs后PD-1诱导的脾肿大症状显著缓解。这些结果说明,MDSCs可能是内源性PD-1介导前列腺癌免疫抑制的关键细胞。
四、USP7是PCa中PD-1的重要稳定调节剂
PCa细胞系PC3中的PDCD1 mRNA表达与PD-1蛋白表达并不一致,推测蛋白质稳定性是导致这一现象的关键因素。泛素化/去泛素化系统是内源性蛋白质稳定化的常见机制,为了鉴定调控PD-1稳定性的潜在去泛素化酶,研究团队从Jurkat细胞中免疫沉淀PD-1-Flag蛋白,并通过质谱分析鉴定相互作用蛋白。发现USP7可能在PD-1去泛素化调控中发挥关键酶作用,通过免疫沉淀分析截短的USP7蛋白,观察到其C端UBL结构域是PD-1与USP7结合的关键区域。敲低USP7后,PD-1的泛素化水平显著升高,通过对USP7活性位点内个关键残基进行定点突变,观察到其对PD-1的稳定功能被完全破坏,导致PD-1的泛素化水平急剧上升。转染代表蛋白酶体降解信号的Ub-K48后,USP7显著降低Ub-K48水平,而催化失活突变体则丧失该能力。随后分析五种PCa细胞系中的USP7和PD-1蛋白水平,发现两者之间存在显著相关性,免疫沉淀实验也验证了USP7与PD-1在C4-2和Jurkat细胞中的相互作用。
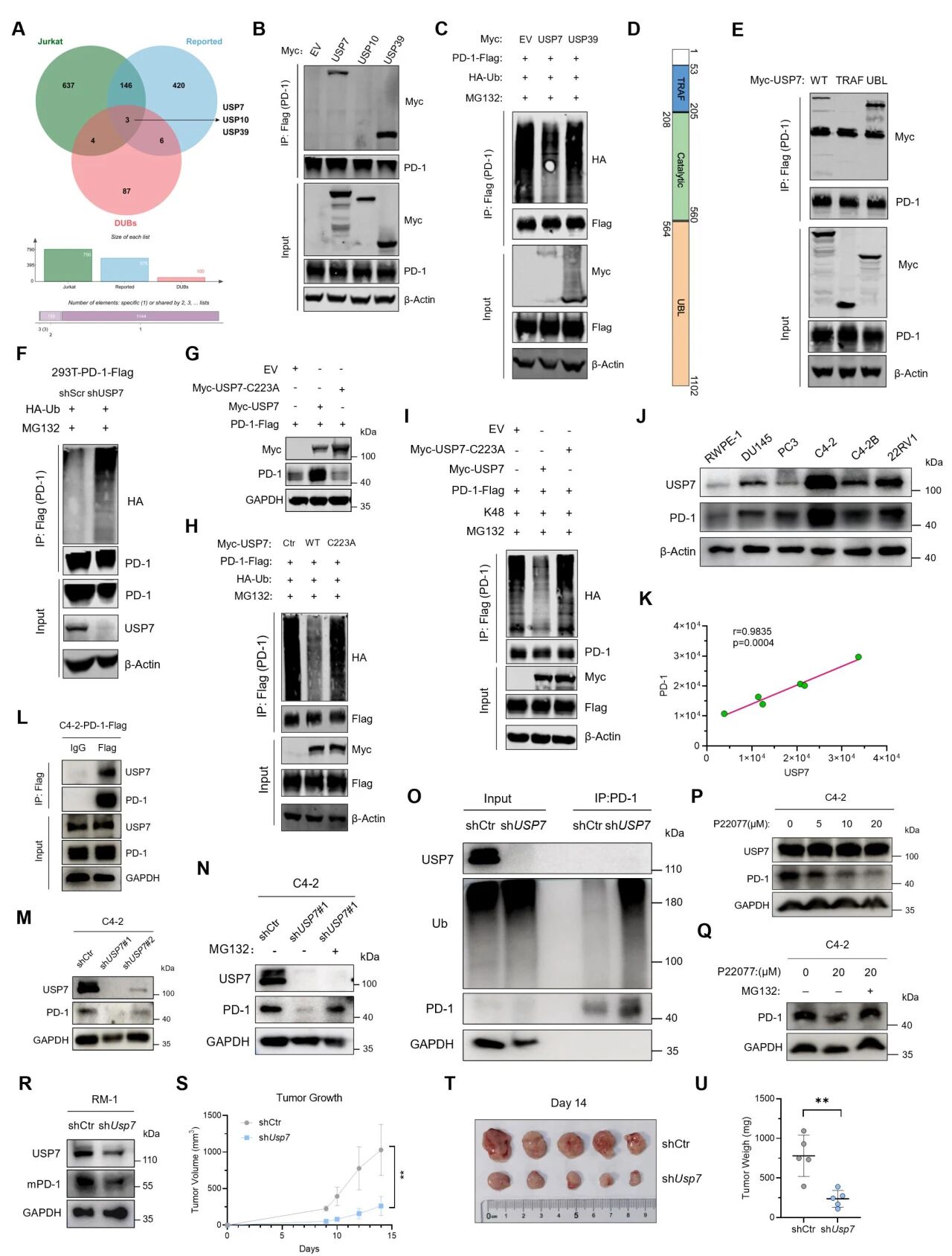
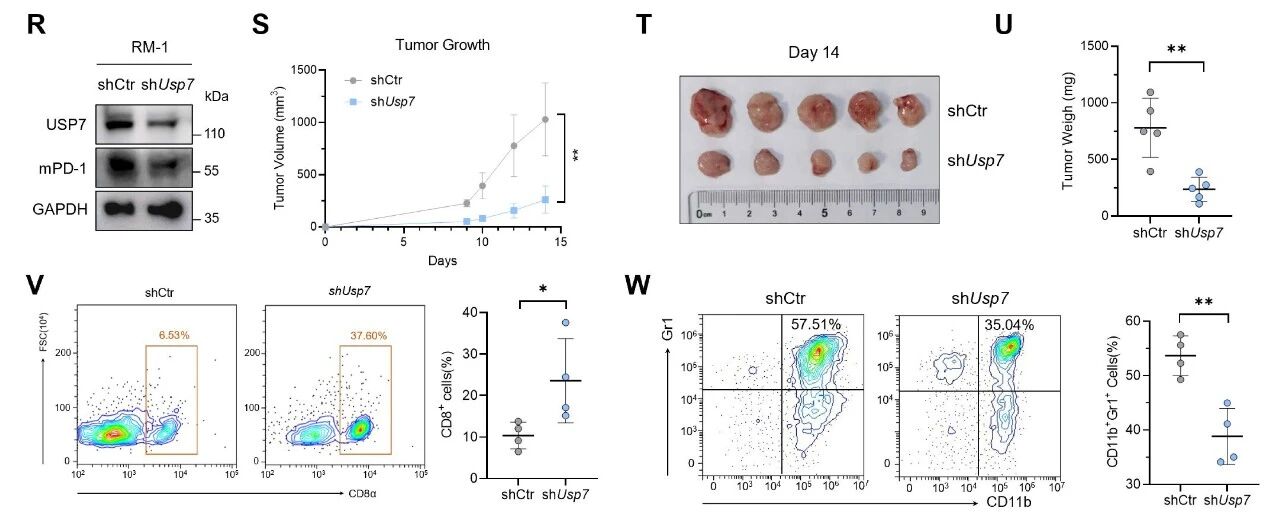
USP7基因敲低持续导致PD-1泛素化水平显著升高,而USP7的抑制剂P22077和P5091能有效降低前列腺癌细胞中的PD-1表达水平。为了验证USP7抑制是否可消除肿瘤来源外泌体介导的PD-1免疫抑制作用,研究使用USP7敲低的前列腺癌细胞进行皮下肿瘤生成实验,发现能显著抑制小鼠前列腺癌细胞的生长,同时伴随CD8+ T细胞浸润显著增加和MDSCs数量大幅减少。
五、靶向抑制USP7使PCa细胞对ICB治疗敏感
为验证USP7在小鼠模型中对MDSCs的主要作用是否通过PD-1依赖机制实现,研究进行了Pdcd1敲除+USP7敲低的联合,以评估其对MDSC调控的潜在叠加效应。皮下肿瘤形成实验显示:单独敲低USP7或敲除Pdcd1均能显著抑制肿瘤进展,其中后者效果更为显著。而联合敲除Pdcd1和USP7相较于单独敲除Pdcd1未能展现出更优的抑瘤效果。流式分析也证实,单独敲除Pdcd1与联合敲除Pdcd1和USP7的肿瘤模型中,MDSC浸润水平相当。因此可以证明,USP7主要通过PD-1介导的机制调控MDSCs。
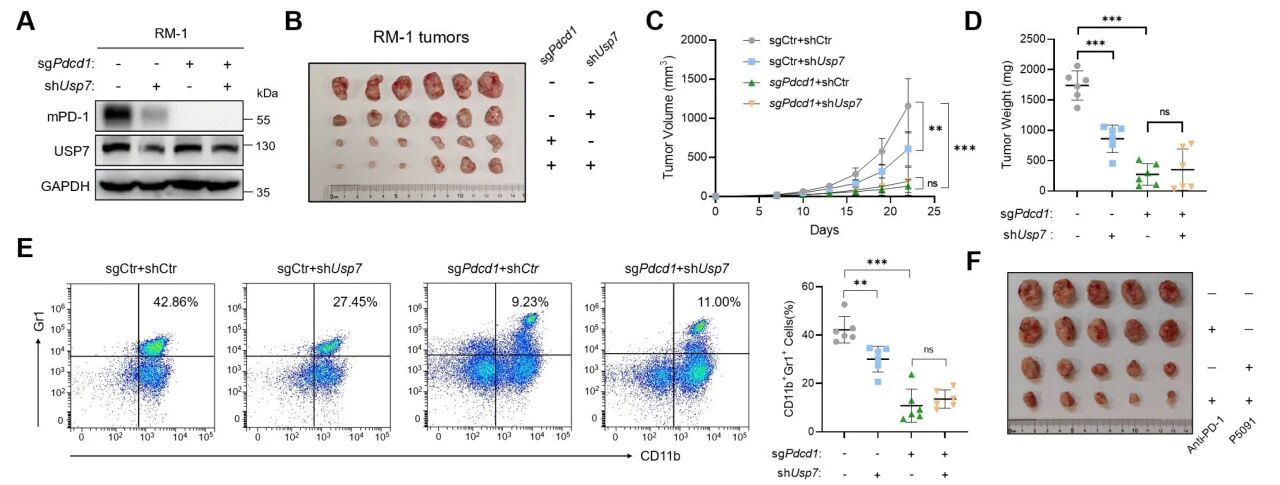
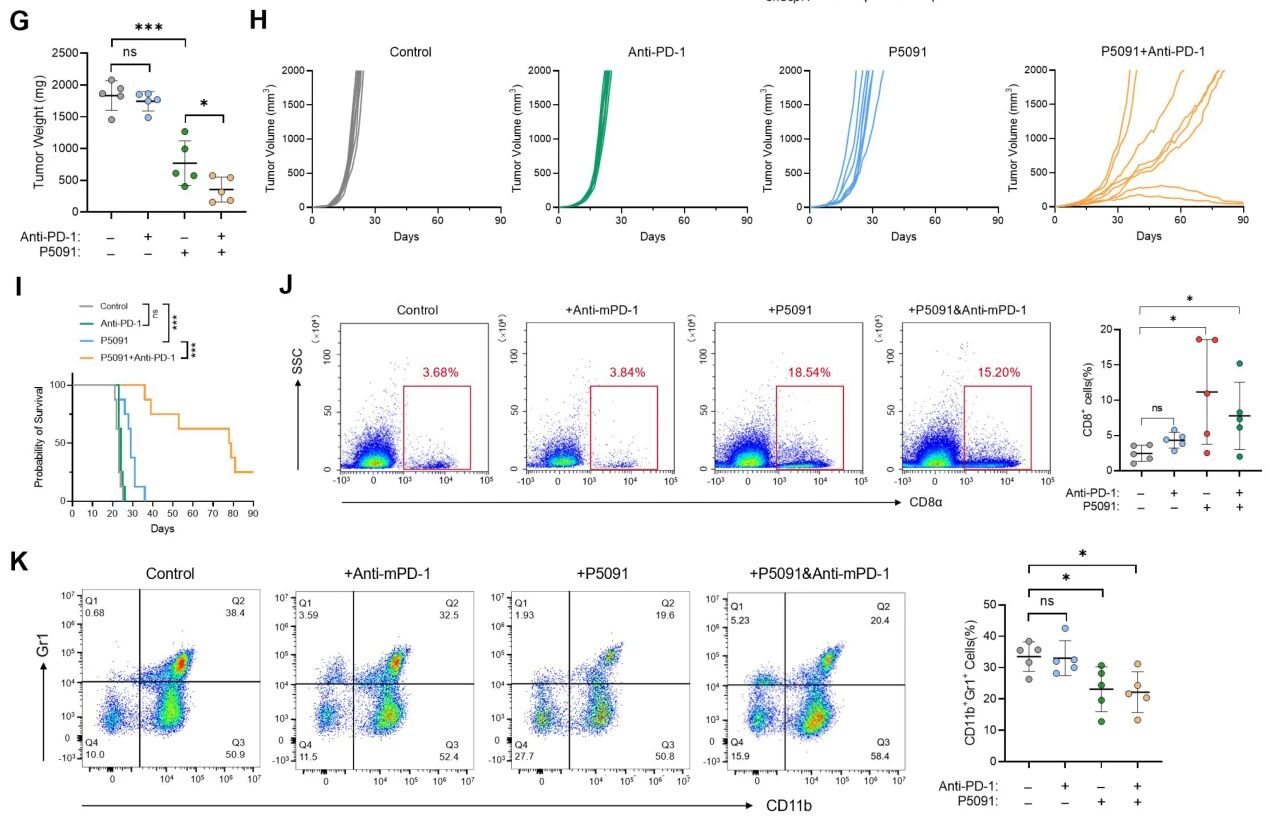
随后,研究评估了USP7抑制剂P5091与PD-1单克隆抗体联合治疗PCa在小鼠模型中的疗效,发现当P5091与PD-1单抗联用时,能显著抑制前列腺癌进展并提高免疫功能正常雄性C57BL/6J小鼠的总体生存率,同时伴随CD8+ T细胞浸润增加和MDSCs(尤其是PMN-MDSCs)浸润减少。可以证实USP7敲低介导的PD-1降解在上述荷瘤小鼠模型中起关键作用。综上所述,本研究揭示前列腺癌中的内源性PD-1通过外泌体运输介导JAK-STAT3激活,进而驱动MDSCs生成与活化。这些发现凸显了靶向USP7开发小分子抑制剂作为前列腺癌治疗新策略的巨大潜力。
研究结论
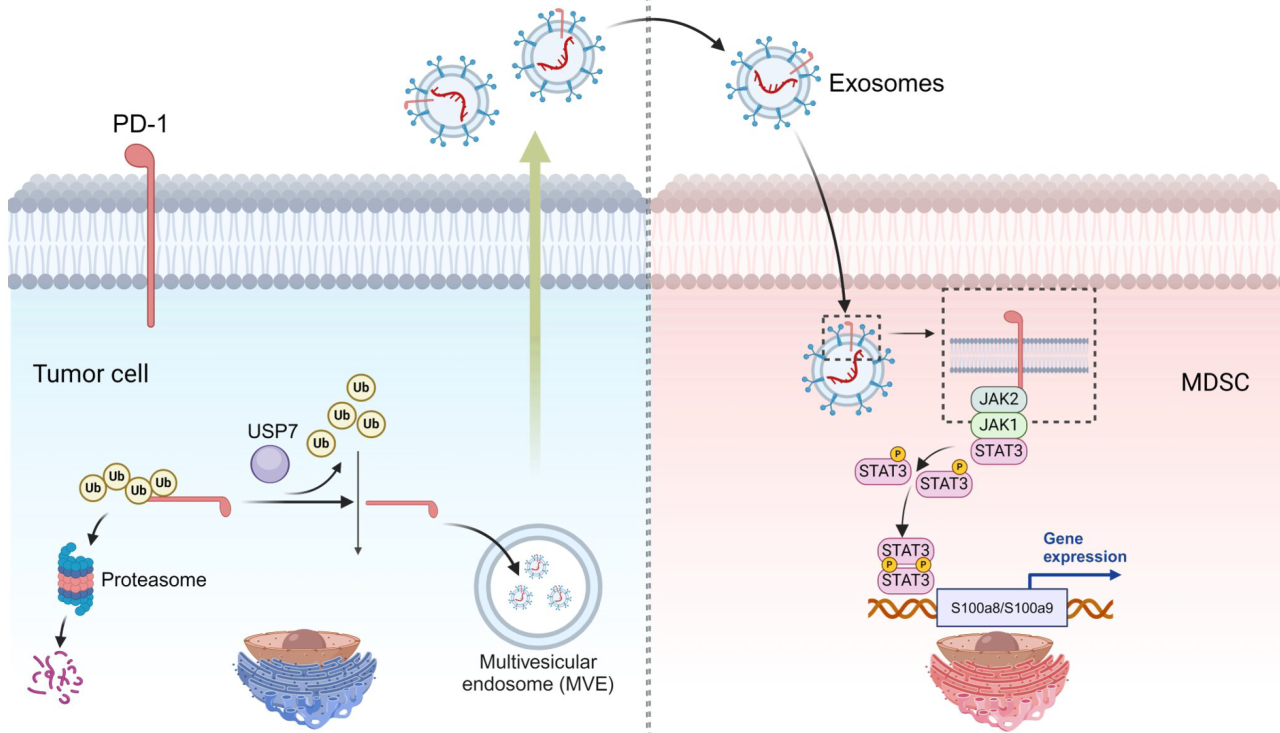
本文研究了PD-1在PCa中的表达和功能,并揭示了对肿瘤微环境的影响。癌细胞中PD-1的表达与Gleason分级和转移呈正相关,但与PCa患者的CD8+ T细胞浸润呈负相关。PCa细胞在外泌体中分泌PD-1,通过激活JAK/STAT3信号传导增强MDSCs的活性。激活的MDSC反过来减少了CD8+ T细胞在肿瘤内的浸润,促进了肿瘤免疫逃逸。泛素特异性蛋白酶USP7诱导去泛素化,提高PCa中PD-1的丰度,USP7抑制使PCa肿瘤对抗PD-1抗体治疗敏感。鉴于目前免疫治疗方法对PCa的疗效一般,抑制携带PD-1的外泌体分泌或USP7功能的策略可能会成为治疗PCa的有前途的免疫刺激干预措施。
因此,本研究阐明了由USP7调控的肿瘤来源PD-1通过外泌体介导的途径激活PMN-MDSCs,从而导致免疫抑制研究为前列腺癌肿瘤微环境的免疫抑制机制提供了新的见解,并为晚期前列腺癌提供了一个新的治疗靶点。
参考文献
[1] Zhang J, Chen W, Chen Y, et al. Prostate Cancer Cells Secrete PD-1 in Exosomes to Enhance Myeloid-Derived Suppressor Cell Activity and Promote Tumor Immune Evasion. Cancer Res. 2025 Jul 23.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
