自1885年波尔多液问世以来,铜基杀菌剂(CBACs)在农业上应用已超过130年。传统观点认为其作用仅仅是“物理屏障”和“直接杀菌”。然而,近期武汉大学储昭辉教授团队在Journal of Advanced Research(IF=13.0)上发表了题为“The CPK3-mediated cytosolic–nuclear translocation of bHLH107 recruits HY5 to regulate the Cu2+-triggered upregulation of ACS8”的研究论文,揭示了一个惊人的事实:低浓度的铜离子本身就能作为信号,通过磷酸化修饰触发植物自身强大的免疫防御系统。今天,我们将深入解析这一研究,探讨 Cu2+ 如何通过 CPK3-bHLH107-HY5-ACS8 这一核心模块,实现从离子信号到抗病能力的跨越。
北京青莲百奥生物科技有限公司为文章提供了磷酸化修饰检测服务。

研究背景交代
铜是植物生长必需的微量元素,但过量则产生毒性。在植物病害防治中,低浓度的铜离子(低于 200 μM)并不能直接抑制细菌的生长,但却能显著增强植物的抗病性。
已知乙烯合成限速酶基因 ACS8 的表达上调是铜诱导免疫的关键,且其启动子区域存在铜响应元件(CuRE)。但问题在于:谁感知了铜信号?谁将信号从胞质传导至核内?谁最终开启了转录大门?
样本与技术流程
实验模型:
以拟南芥(Arabidopsis thaliana)为核心模型,涵盖了野生型(Col-0)、多种 T-DNA 插入突变体(bhlh107、cpk3、hy5、acs8)以及基因回补株系。
技术:
磷酸化修饰组学 & 转录组学:筛选铜响应的关键蛋白及修饰。
DNA Pull-down质谱:捕获与 ACS8 启动子结合的转录因子。
互作验证:酵母单杂交(Y1H)、双分子荧光互补(BiFC)、免疫共沉淀(Co-IP)和体外 Pull-down。
功能验证:ChIP-qPCR、EMSA、定点突变、亚细胞定位观察。
研究结果
1. 核心转录因子的锁定:bHLH107
研究首先通过遗传学实验证明,删除ACS8启动子中的CuRE元件,会完全消除铜离子诱导的ACS8表达和对病原菌Pst DC3000的抗性(图1A, B),证实CuRE是必不可少的。随后,通过DNA pull-down和质谱分析,从候选蛋白中筛选出bHLH107,并通过电泳迁移率变动分析和染色质免疫共沉淀实验,分别在体外和体内证实bHLH107能够直接、特异地结合到CuRE序列上,且这种结合在铜离子处理后显著增强(图1C, G)。初步的荧光素酶报告基因实验也显示bHLH107能激活由CuRE驱动的报告基因表达。
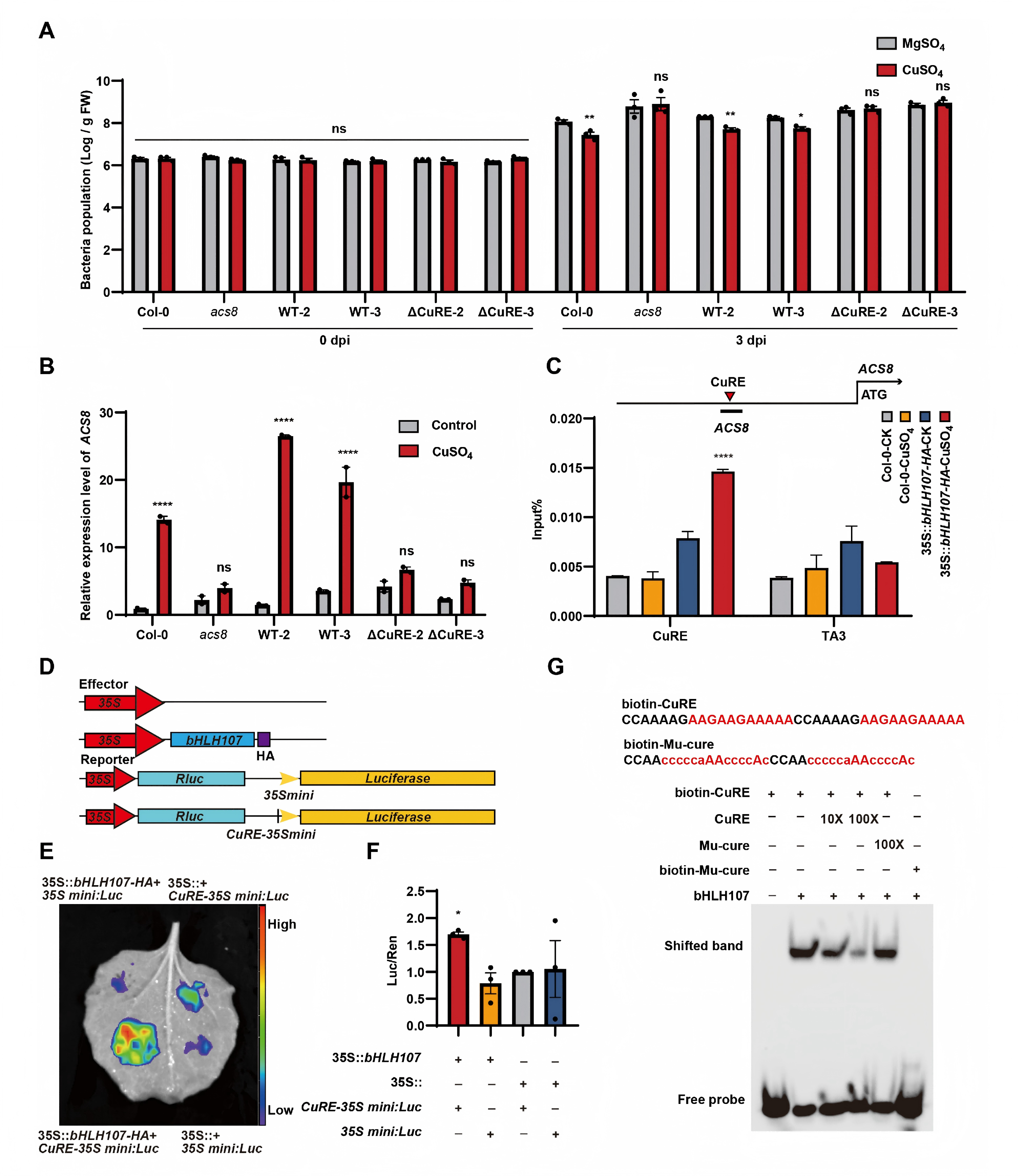 图1. bHLH107 直接结合 ACS8 启动子中的 CuRE 顺式作用元件
图1. bHLH107 直接结合 ACS8 启动子中的 CuRE 顺式作用元件
2. bHLH107正向调控铜离子触发的免疫反应
利用两个T-DNA插入突变体(bhlh107-1, bhlh107-2)和一个CRISPR基因编辑突变体(bhlh107),研究人员发现,这些突变体中铜离子诱导的ACS8表达显著减弱(图2B, E),对Pst DC3000的抗性也明显下降(图2C, F)。而将完整的bHLH107基因回补到突变体中,则可以恢复这些功能(图2B, C)。这直接证明bHLH107是铜离子触发免疫所必需的。此外,转录组分析表明,bhlh107突变导致大量铜离子诱导的防御相关基因(如植物-病原互作、激素信号转导通路基因)表达受阻(图2H-K),进一步从全基因组水平证实了bHLH107的核心调控作用。
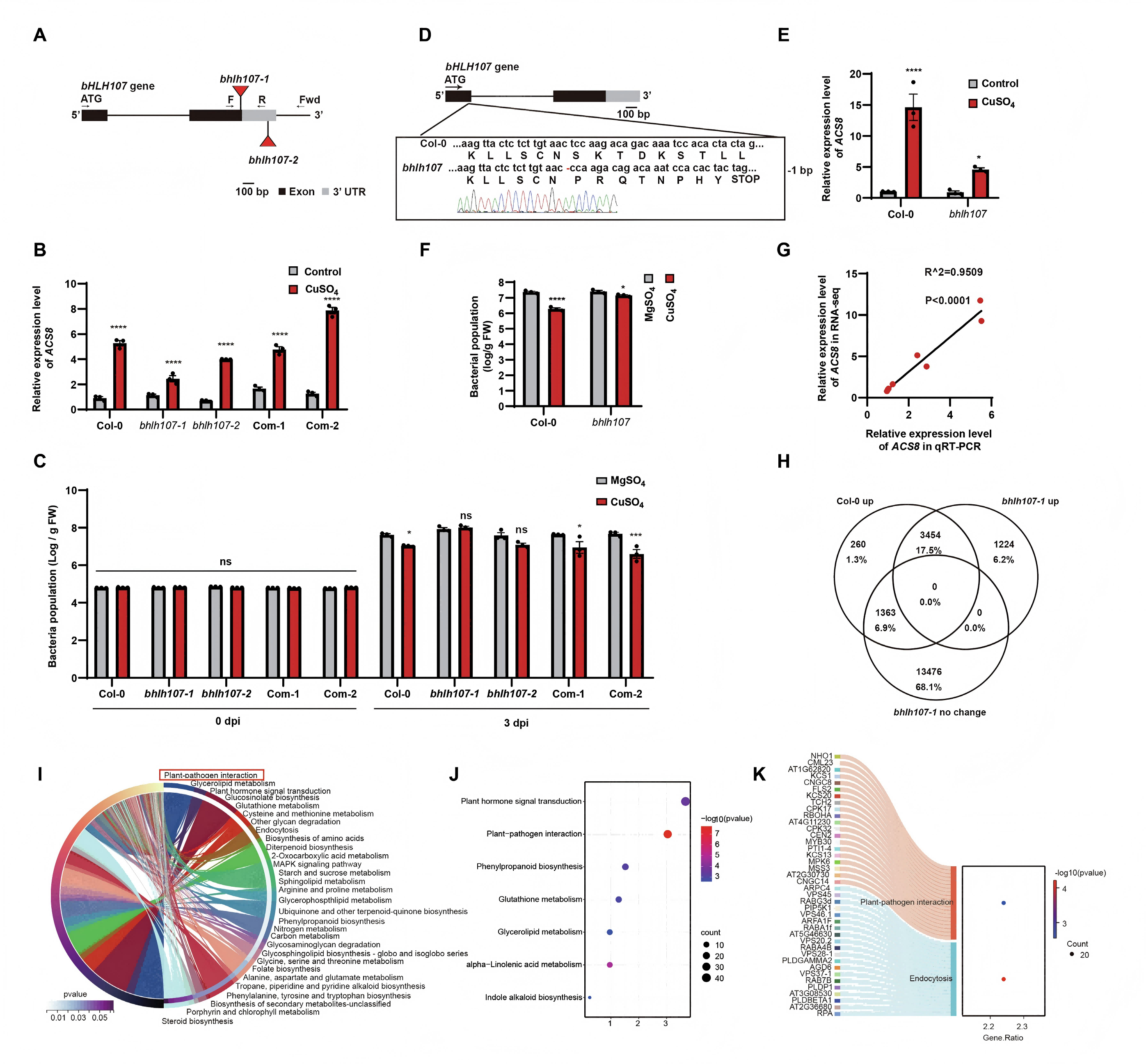 图2. bHLH107 正向调控拟南芥中由 Cu2+ 触发的免疫反应
图2. bHLH107 正向调控拟南芥中由 Cu2+ 触发的免疫反应
3. 铜离子刺激bHLH107发生磷酸化并向细胞核转移
虽然bHLH107的转录本水平受铜诱导,但仅仅过表达bHLH107并不能完全模拟铜离子的免疫增强效果(图3A-C),这表明存在转录后调控。细胞组分分离实验和荧光共聚焦显微镜观察显示,在正常情况下,bHLH107蛋白分布于细胞质和细胞核;而铜离子处理后,bHLH107快速从细胞质向细胞核富集(图3D, E)。同时,Phos-tag凝胶电泳检测到铜离子处理增加了bHLH107的磷酸化水平(图3F),提示磷酸化可能驱动了其核定位变化。
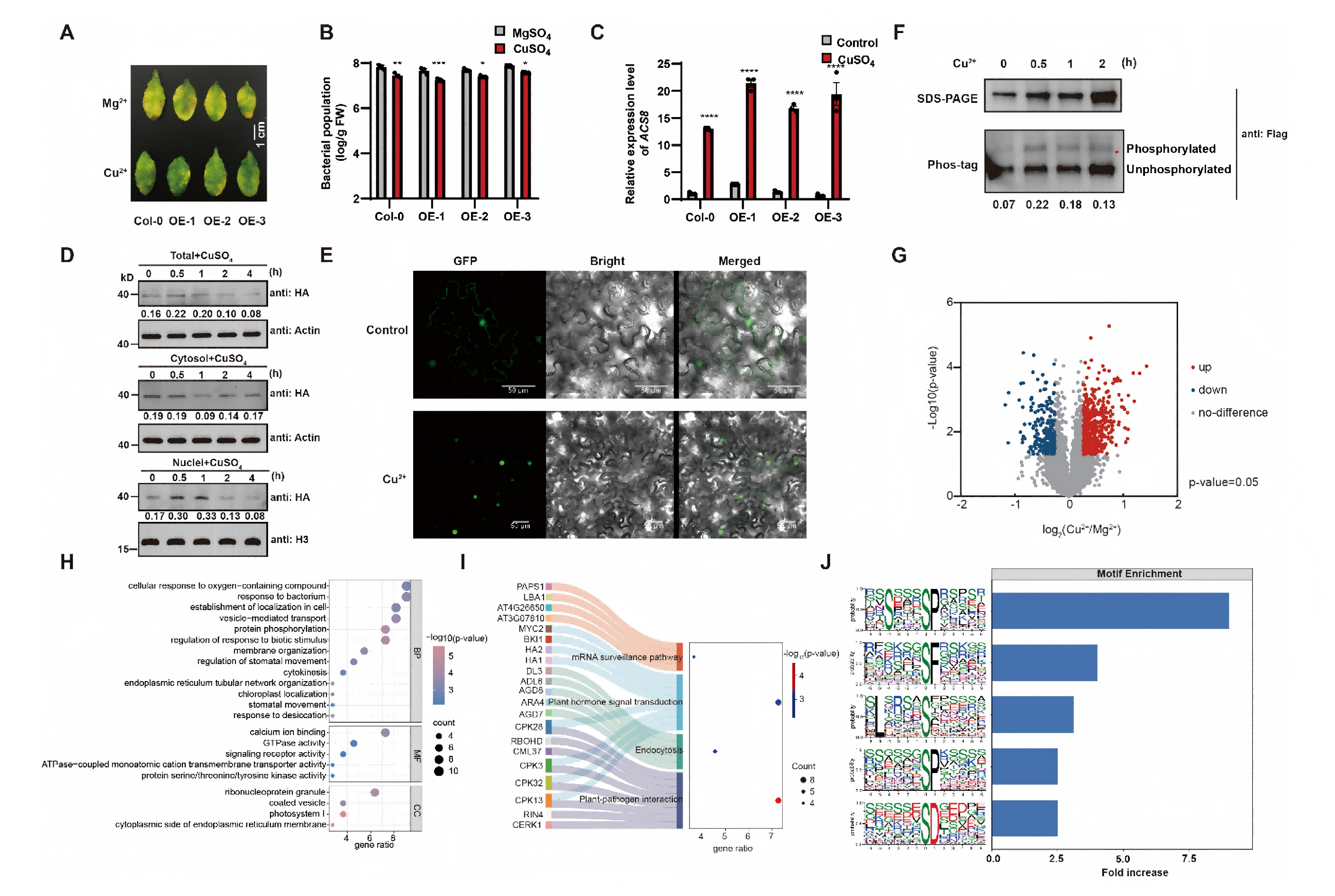 图3.Cu2+刺激 bHLH107 发生磷酸化并向细胞核转位
图3.Cu2+刺激 bHLH107 发生磷酸化并向细胞核转位
4. 钙依赖蛋白激酶CPK3磷酸化bHLH107,介导其核转位
通过磷酸化蛋白质组学和IP/MS分析,研究团队将目光锁定在钙离子传感器CPK3上(图4A)。实验证实CPK3与bHLH107存在物理互作(图4C-E),且cpk3突变体同样表现出铜离子诱导的ACS8表达和抗病性缺陷(图4F-H)。
磷酸化位点鉴定验证:体外激酶实验和LC-MS/MS分析确定,CPK3能够磷酸化bHLH107的第62位和第72位丝氨酸(图5A-E),图5C给出了Ser72磷酸化肽段的质谱二级谱图作为修饰存在的直接证据。
功能验证:将这两个位点突变为模拟磷酸化的天冬氨酸(S62/72D)后,bHLH107主要定位于细胞核,并能持续激活下游报告基因和增强抗病性;反之,突变为无法磷酸化的丙氨酸(S62/72A)后,bHLH107则滞留在细胞质,且其转录活性和介导的抗病性显著降低(图5F-J)。
依赖关系:在CPK3突变体背景下,铜离子无法诱导bHLH107的核积累(图5K, L)。这些结果共同证明,CPK3通过磷酸化bHLH107的Ser62和Ser72,驱动其从细胞质向细胞核转运,从而激活其转录功能,是铜信号传递中的关键步骤。
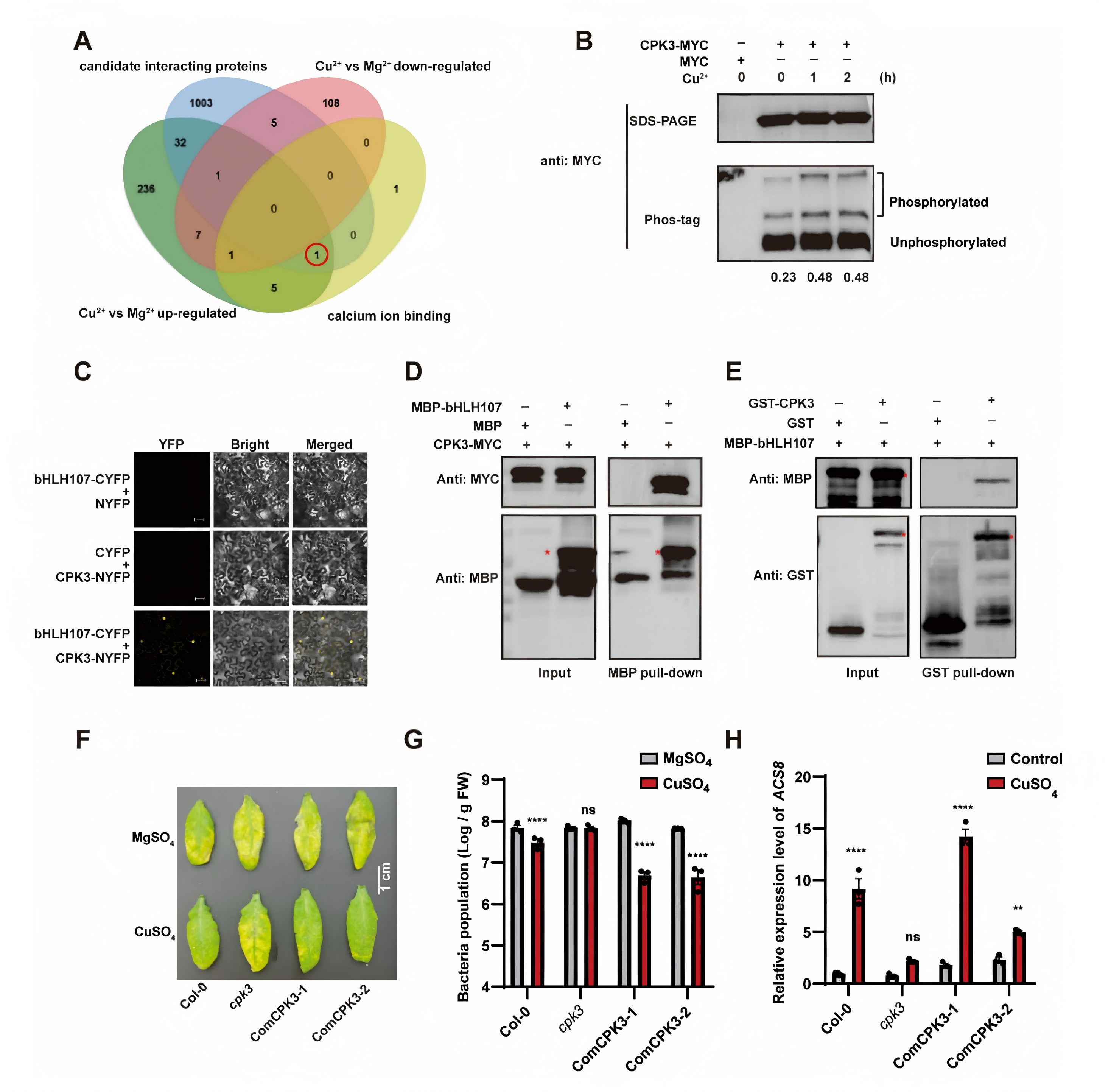
图4. CPK3与bHLH107相互作用并参与Cu2+触发的免疫
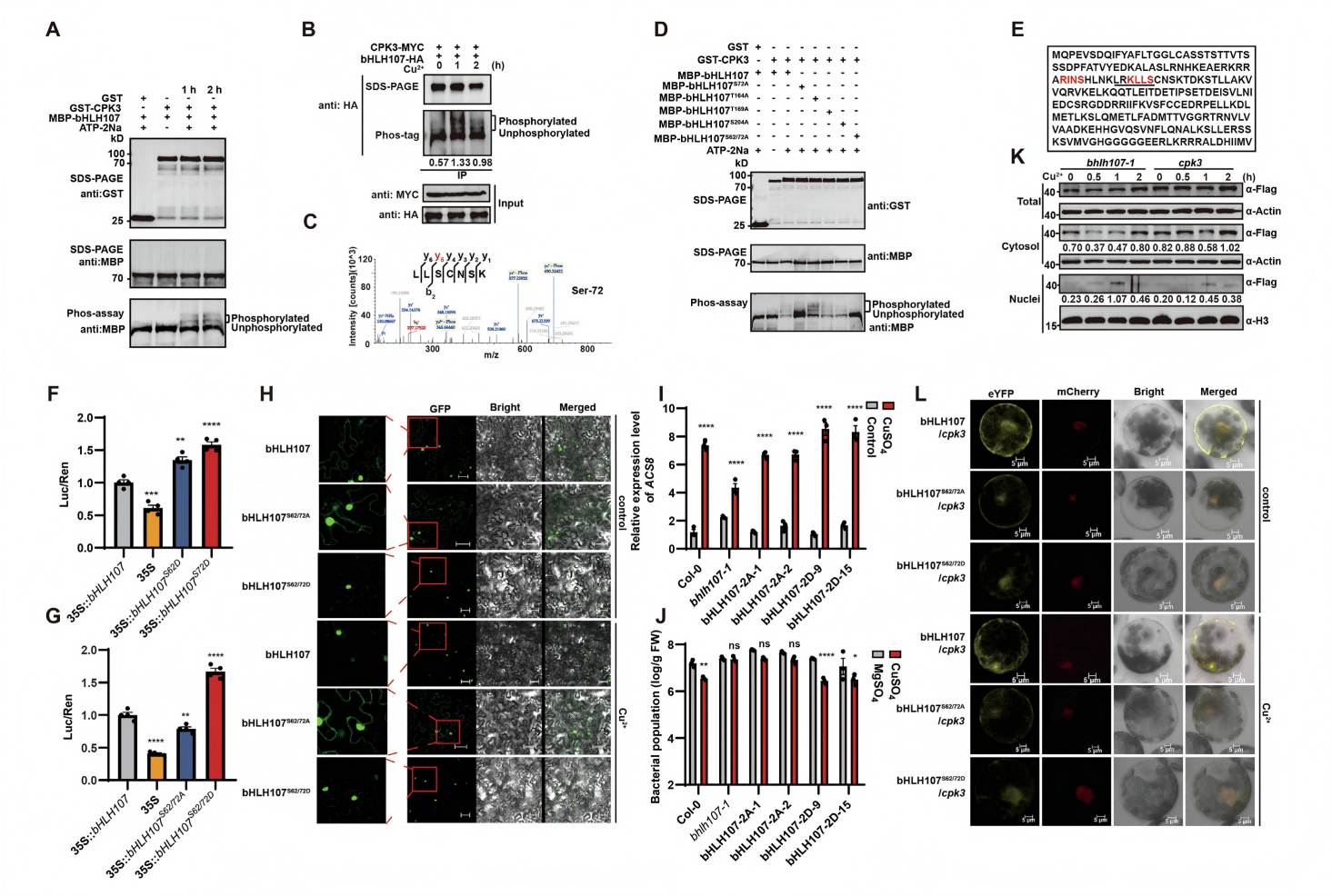
图5. CPK3 磷酸化 bHLH107 的Ser62/72,促进其核积累和转录激活功能
5. 转录因子HY5作为bHLH107的共激活子,协同放大免疫信号
在细胞核内,bHLH107并非独自工作。研究发现它与光信号核心转录因子HY5相互作用(图6A-D)。HY5功能缺失突变体(ks50)对铜离子诱导的抗病性减弱(图6F)。结合机制为HY5不结合CuRE,而是直接结合在ACS8启动子上的ACGT元件(图6I-L)。而且,在HY5缺失的背景下,即使过表达bHLH107,其与CuRE的结合能力也大幅下降(图6M)。这表明,HY5作为bHLH107的“共激活子”,通过直接结合邻近的DNA位点,稳定并增强了bHLH107与CuRE的结合,从而协同放大ACS8的转录激活信号。
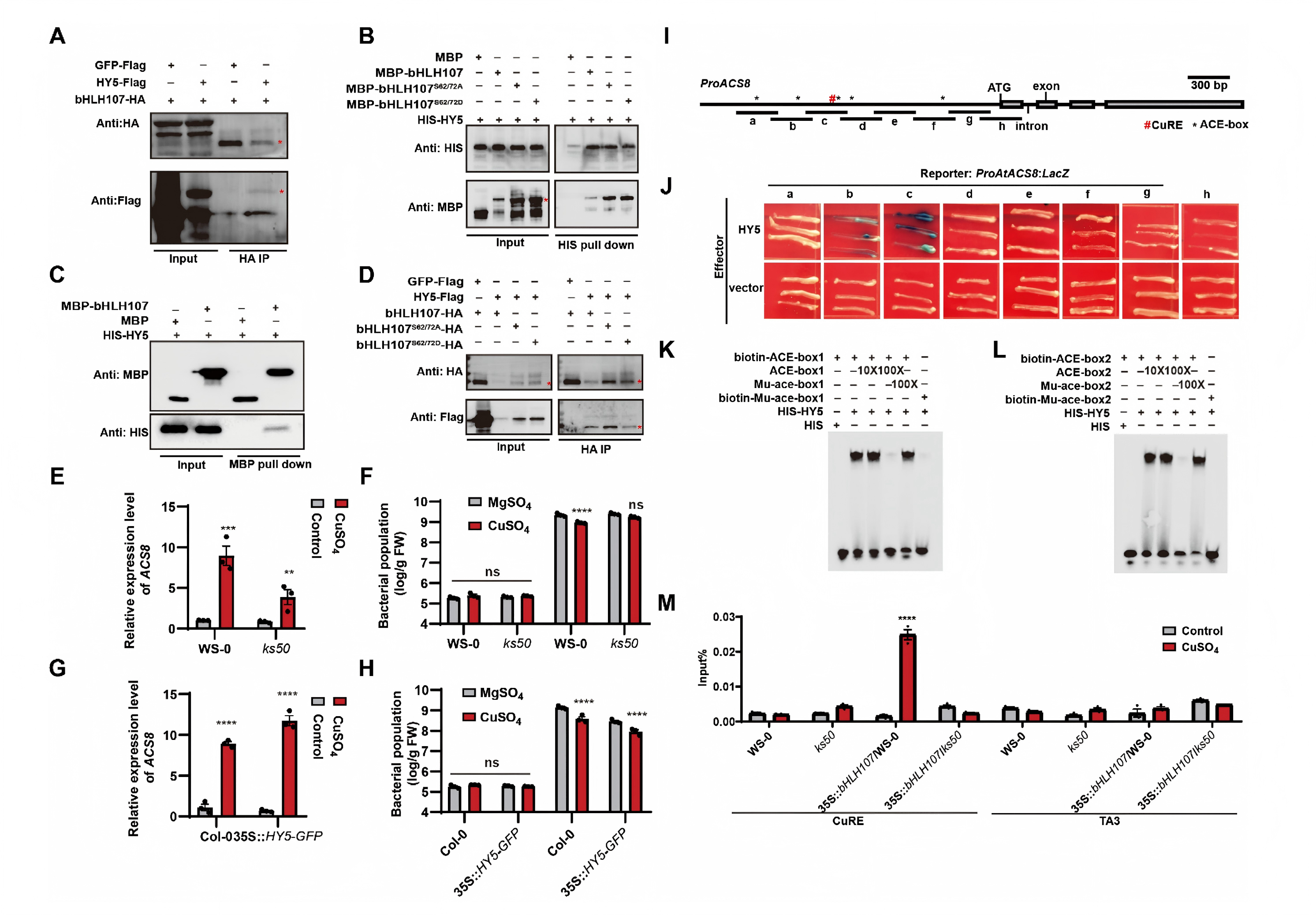
图6. HY5 与 bHLH107 发生物理相互作用并参与Cu2+诱导的防御反应
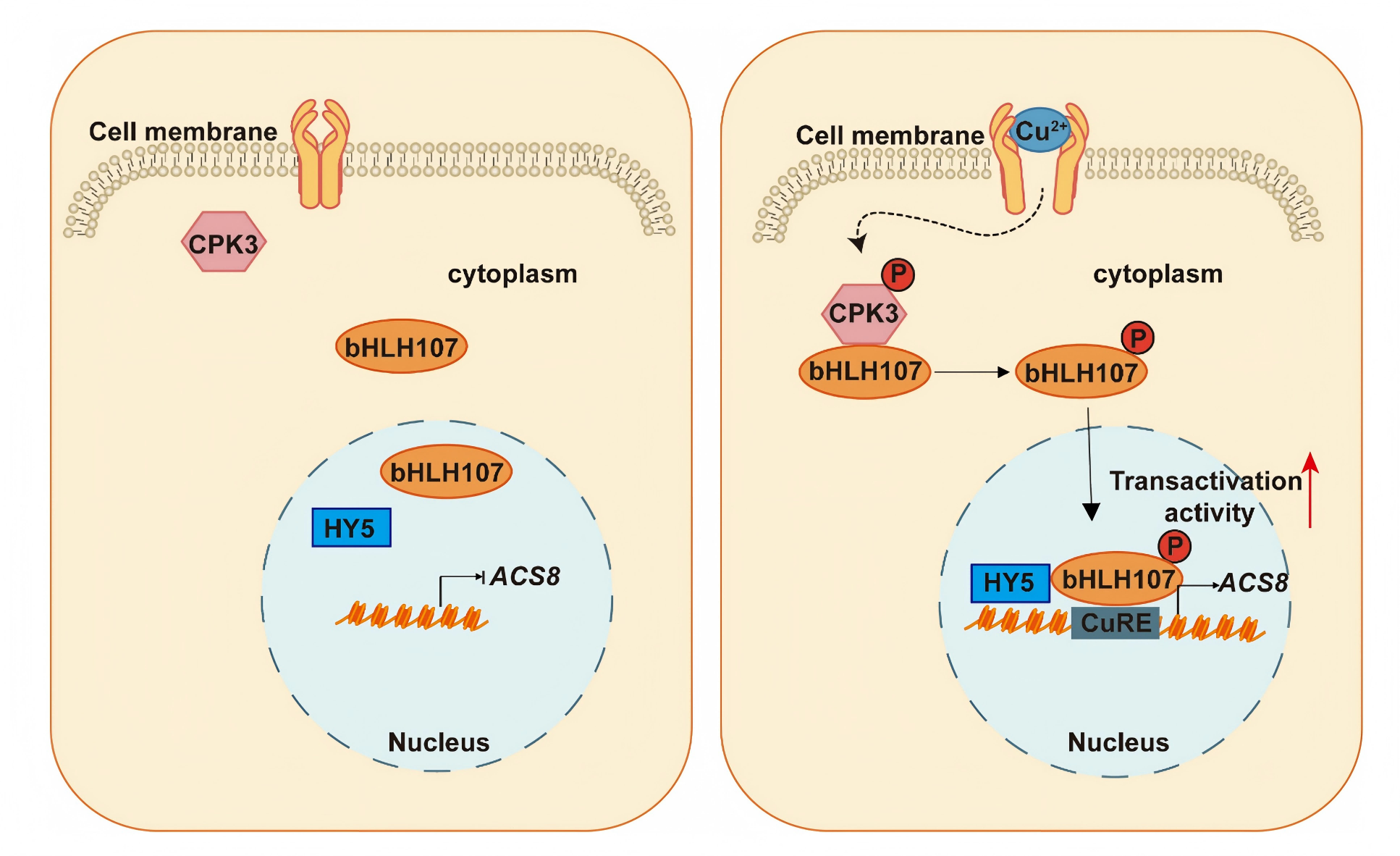
图7. 总结:CPK3-bHLH107-HY5 模块调控Cu2+触发的植物免疫
总结
该研究构建了一个完整的信号通路图谱(图7):
感应期:微量铜离子刺激导致细胞内钙离子信号波动,激活 CPK3 激酶;
传导期:CPK3 磷酸化 bHLH107 的 Ser62/72 位点,驱动其从胞质进入细胞核;
执行期:进入核内的 bHLH107 招募 HY5,共同结合在 ACS8 启动子上;
效应期:乙烯合成基因大量表达,植物免疫系统全面“唤醒”,成功抵御病原菌入侵。
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
