塑料污染已成为环境和公共健康的一大威胁。纳米塑料(NPs)可通过呼吸、饮食、皮肤接触等途径进入人体,并在通过血液循环在组织器官中积累,对健康造成长期影响。
蛋白冠(protein corona)指纳米材料进入生物环境(如血液等体液)后其表面吸附的一层或多层蛋白所组成的结构。蛋白冠的形成不仅改变纳米粒子的表面特性,还影响其稳定性、细胞摄取、组织分布及潜在的毒性和生物效应。
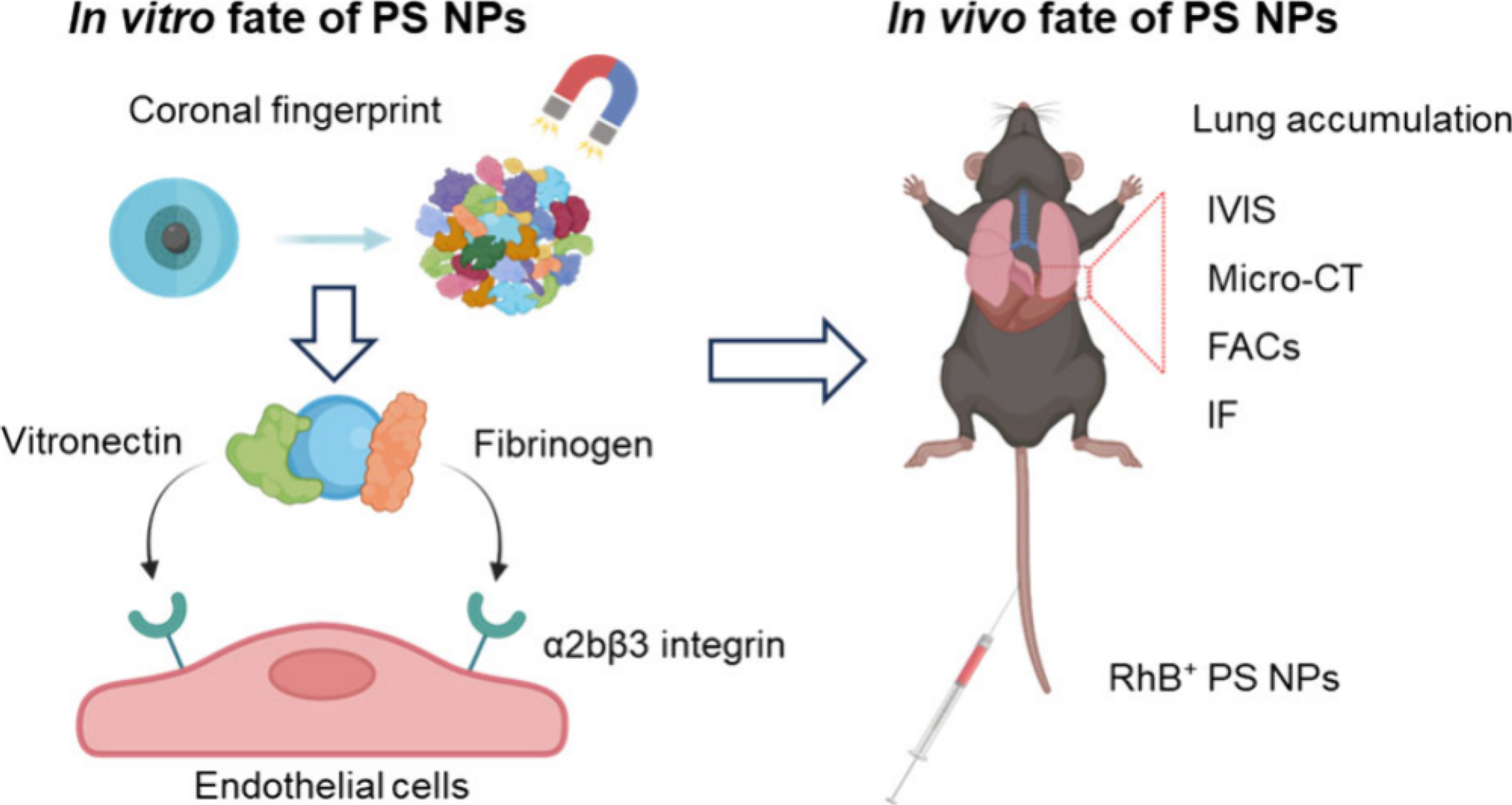
2024年10月3日,中国科学院高能物理研究所中国科学院纳米生物效应与安全性重点实验室王黎明、张智勇团队携手青莲百奥研发团队,采用磁性纳米材料合成技术合成带有铁核的聚苯乙烯纳米塑料(PS NPs),通过磁分离技术高效鉴定了铁核PS NPs的蛋白冠组成,并通过同步辐射微CT(SR-micro-CT)成像技术鉴定了铁核PS NPs在肺内的积累,并对其肺内积累机制进行了深入探究。

文章题目:Preferred Lung Accumulation of Polystyrene Nanoplastics with Negative Charges.
发表期刊:Nano Letters
影响因子:9.6
发表时间:2024年10月3日
发表单位:中国科学院高能物理研究所&北京青莲百奥生物科技有限公司
合成带有铁核的PS NPs并构建两种表面功能化形式:羧基化(COOH-NPs)和氨基化(NH2-NPs)。通过透射电子显微镜(TEM)和流体动力学直径测量确定PS NPs的平均尺寸并测量其表面电荷。使用X射线衍射(XRD)和傅里叶变换红外光谱(FTIR)确认铁核的晶体结构和化学成分。磁性质表征显示铁核PS NPs的饱和磁化值在快速磁分离中稳定。
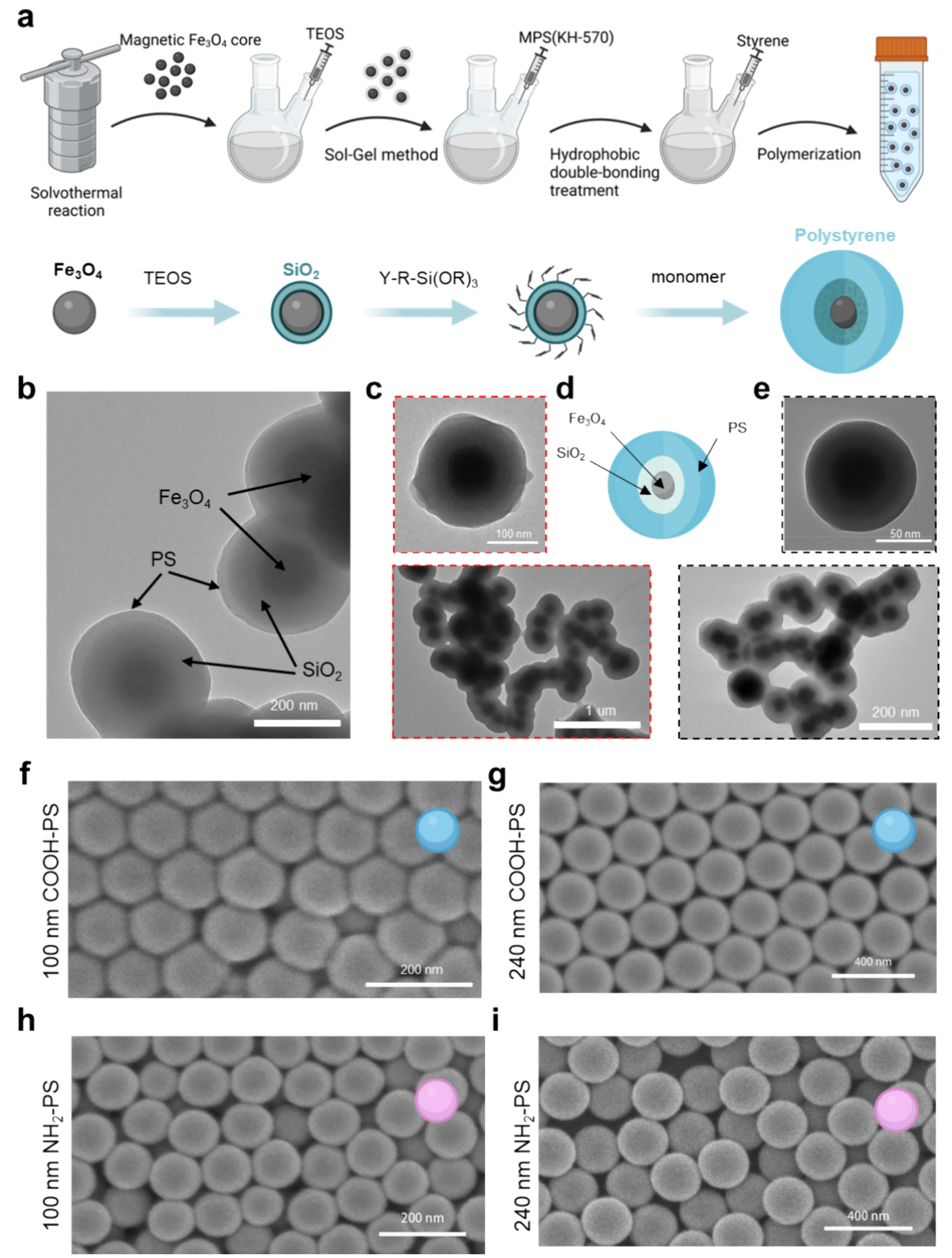
图1 铁核聚苯乙烯纳米颗粒的合成与表征
磁分离法在蛋白冠的鉴定中具有以下四大优势:
简单高效:通过外加磁场实现快速分离,高效、高通量,易于自动化、标准化;
减少损伤:不涉及高速离心等可能导致蛋白质结构变化或破坏的步骤,有助于保持蛋白冠的完整性和生物活性;
高选择性:特异性分离磁性颗粒,支持多次洗涤;
高分辨率成像:结合同步辐射微CT(SR-micro-CT)等高分辨率成像技术,可提供磁性颗粒在体内分布的三维可视化,有助于准确示踪。
使用磁分离法研究人血浆蛋白与纳米塑料的相互作用,发现NPs的大小和表面修饰对蛋白冠中玻连蛋白(vitronectin)的富集有显著影响。较大的NPs表面积更大,提供更多蛋白质结合位点,促进玻连蛋白吸附。
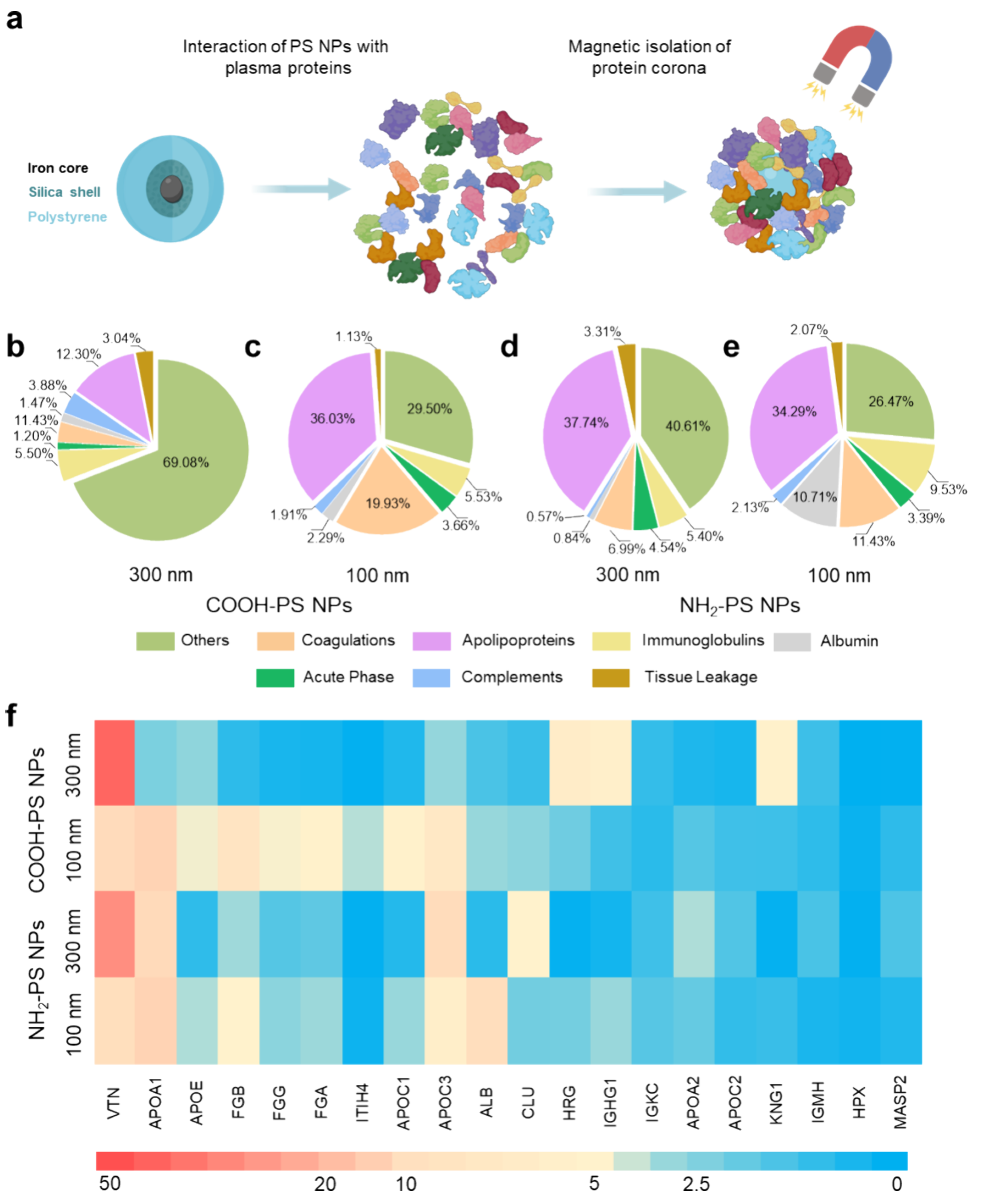
图2 铁核PS NPs中蛋白冠成分的磁分离与鉴定
通过C57BL/6J小鼠体内实验,发现静脉注射50 mg/kg PS NPs最初在肝中积累,带负电荷的COOH-NPs在注射后30min内显著积累在肺部,而带正电荷的NH2-NPs则没有这种积累。直径100 nm的COOH-NPs显示出更有效的肺部积累,表明带负电荷的纳米颗粒能够更有效地穿越血管内皮屏障。
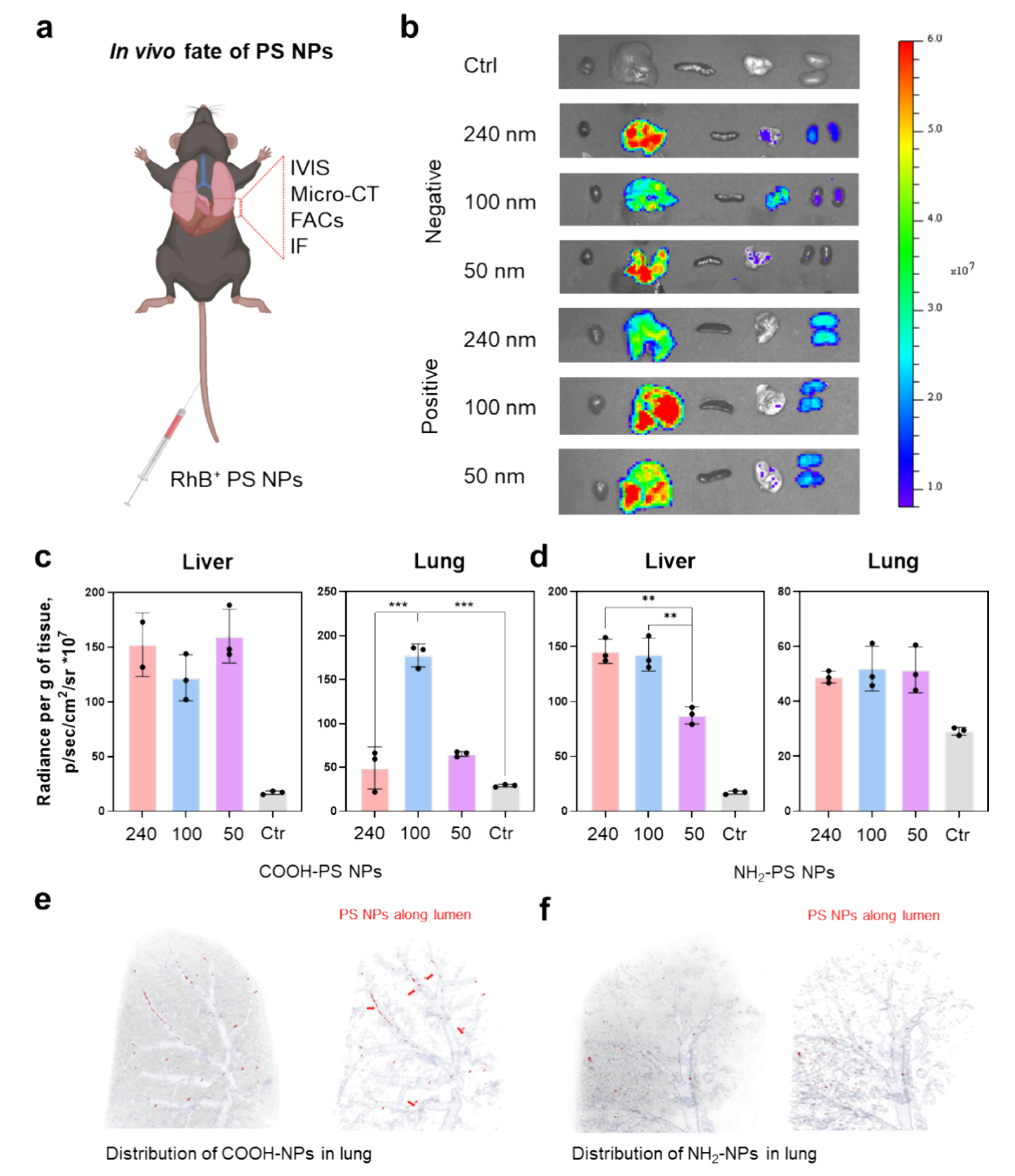
图3 PS NPs的体内分布和细胞摄取
关注蛋白冠中含量最丰富的玻连蛋白,发现玻连蛋白吸附到不同PS NPs表面时会发生不同构象变化,可能导致其结构和取向的变化。玻连蛋白吸附到COOH-NPs上后构象变化较少,导致其细胞摄取相比NH2-NPs更低。
使用流式细胞术确定100nm PS NPs注射后30min内在小鼠肺部的分布,结果显示COOH-NPs在肺组织中的积累水平显著高于NH2-NPs。免疫荧光实验观察到PS NPs与肺内皮细胞上的CD41/CD61整合素受体的共定位,表明玻连蛋白通过整合素受体介导的途径促进了COOH-NPs在肺细胞中的积累。

纳米塑料的表面特性,特别是电荷和蛋白冠组成,对其在体内的分布和积累模式有显著影响。这些发现对于理解纳米塑料的生物命运和潜在健康风险具有重要意义,也为未来纳米塑料的风险评估和安全塑料材料的开发提供了重要的科学依据。
青莲百奥致力于基于磁珠的蛋白质组学技术研究,深耕蛋白冠形成机制与磁性材料研发,独家推出四大磁珠试剂盒——MagicOmics DMB血浆低丰度蛋白富集磁珠试剂盒、MagicOmics MMB微量/通用型蛋白质组学磁珠试剂盒、MagicOmics EMB外泌体富集磁珠试剂盒、MagicOmics PEB磷酸化肽段富集磁珠试剂盒,助力高通量、自动化、标准化蛋白质组学研究,简单便捷的操作方式让蛋白质组学的大门向所有研究者敞开!
